Corrigé chimie
Exercice 1 :
Solution tampon
L’acide benzoïque est un acide faible :
Pour un acide fort : $pH=-log c$ ; pour un acide faible $pH>-log c$
Cas de l'acide benzoïque : -$log c= - log 2,5 10^{-2} =1,6$ ;
$pH$ mesuré $= 2,9$ ; l'acide benzoïque est donc un acide faible.
Coefficient d'ionisation
$\begin{array}{rcl}
\alpha &=& [H_{3}O^{+}]/C_{B}\\&=&10^{-2,9} / 2,5 10^{-2}\\&=&
\end{array}$
Coefficient d'ionisation "$alpha_{1}$" : facteur de dilution : $F= 1000 / 10 = 100 ; C_{B1}= 2,5 10^{-4} mol/L \alpha = [H3O^{+}]/C_{B1} = 10^{-pH} / C_{B1} = 10^{-3,9} / 2,5 10^{-4} = 0,50$.
Par dilution, un acide faible se rapproche d'un acide fort ( la dissociation de l'acide faible augmente par dilution)
Coefficient d'ionisation "$\alpha_{2}$" : facteur de dilution : $F = 200 / 100 = 2 ;
$\begin{array}{rcl}
C_{B2} &=& 1,25 10^{-4} mol.L^{-1}\alpha_{2}\\&=&[H3O^{+}]/_{CB2}\\&=&10-pH\, CB2\\&=&10^{-3,25} /,1,25 10^{-2}\\&=&0,045
\end{array}$
Quantité $nb$ d'ion oxonium résultant de l'ionisation de l'acide benzoïque dans ce mélange :
$\begin{array}{rcl}
n_{B}&=&10^{-pH}*(0,1+0,1)\\&=&10^{-3,25} *0,2\\&=&1,12 10^{-4} molC6H5COOH + H2O\\&=&H_{3}O^{+}+C_{6}H_{5}COO^{-}
\end{array}$
en ajoutant un acide ( des ions oxonium) on déplace l'équilibre précédent vers la gauche.
$pH$ d'une solution tampon qui contient $0,01 mol$ d'acide benzoïque ( $K_{a} = 6,6 10^{-5})$ et $0,01 mol$ de benzoate de sodium
$\begin{array}{rcl}
pH&=&pK_{a} + log ([C_{6}H_{5}COO^{-}]/[C_{6}H_{5}COOH]
\end{array}$
Caractéristiques d'une solution tampon :
Le $pH$ ne varie pas par dilution modérée; les variations de $pH$ lors de l'ajout modéré d'une quantité d'ion oxonium ou hydroxyde sont négligeables.
Exercice 2 :
Précipitation
2.1. Calcul du produit des activités relatives et comparaison avec $K_{s}$:
Dans le mélange les concentrations en $Na_{2}CO_{3}$ et en $MgCO_{4}$ ne sont plus les mêmes que dans les solutions initiales,puisque l'augmentation du volume $(O,8L+0,2L=1L)$ provoque une dilution des deux solutés.
Les nouvelles concentrations des ions intéressants sont : $[CO_{3}^{2-}]=2,O.10^{-2}\times (0,8/ 1)=1,6.10^{-2}$
$[Mg^{2+}]=2,O.10^{-2}\times (0,8/ 1)=4,0.10^{-3}$
et le produit des activités relatives vaut: $P=[CO_{3}^{2-}][Mg^{2+}]=6,4.10^{-5}$
$P$ est supérieur à $K_{c}$ et doit donc se former un précipité de $MgCO_{3}$.
b. Masse du précipité
La quantité de $MgCO_{3}$ qui précipité,qu'on désignera par $\varepsilon$ est telle que le produit des concentrations des ions $CO^{2-}_{3}$ et $Mg^{2+}$ restant restant dans un litre de solution soit à $K_{s}$ en notant $[x]$ la quantité $\varepsilon$ divisée par $1 litre$.
Aprés la précipitation,
$P=[CO_{3}^{2-}][Mg^{2+}]=(1,6.10^{-2}6[x])(4,0.10^{-3}-[x])=1,0.10^{-5}$
ce qu'on peut écrire :
$[x]^{2}-2,10^{-2}+5,4.10^{-5}+0$
Cette équation a deux racines :$1,68.10^{-2}mol.L^{-1}$ et $3,2.10^{-3}mol.L^{-1}$.
La première ne peut être retenue puisque la quantité de $MgCO_{3}$ solide formée serait supérieur à la quantité initiale d'ions $CO^{-2}_{3}$.
Si $x=3,210^{-3} mol.L_{-1}$,les concentrations résiduelles dans la solution sont:
$\begin{array}{rcl} [CO^{-2}_{3}]&=&1,6.10^{-2}-3,210^{-3}\\&=&1,3.10^{-2} \end{array}$
$\begin{array}{rcl} [Mg^{2+}]&=&[Mg^{2+}]\\&=&x\\&=&8,0.10^{-4} \end{array}$
(Vérification:le produit de ces deux concentration est bien égal à $K_{s}$).
Le précipité étant constitué par $3,210^{-3}$ mol de $MgCO_{3}(M=84g.mol^{-1})$sa masse est $84g.mol^{-1}\times 3,210^{-3}mol=2,69.10^{-1}g$.
2.3) $Ks = C’_{Mg^{2+}}.C’_{CO_{3}^{-}}$, avec $C’_{Mg^{2+}} = C’_{CO_{3}^{-}} = Ks^{0,5} = C’$.
AN: $C’ = (1,0.10^{-5})^{0,5} = 3,2.10^{-3} mol.L^{-1}$
Par ailleurs,$ C’ = C/2V’$ et donc$ V’ = 2C’/C$
AN: $V’ = 2x 3,2.10^{-3}/2,0.10^{-2}$ d’où $V’ = 3,2.10^{-1} L$
Exercice 3 :
3.1. $X$ est un alcool primaire.
3.2. On a deux isomères.
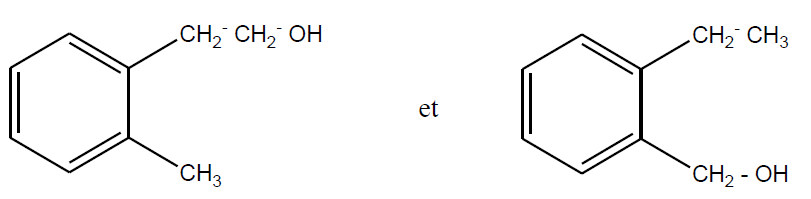
3.3.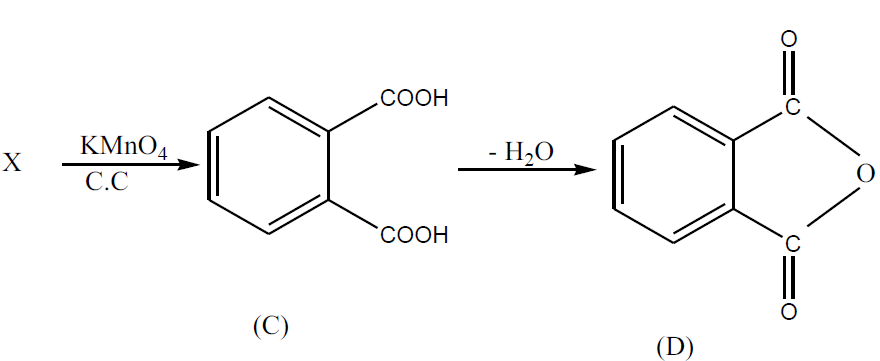
$D$ est l’anhydride phtalique
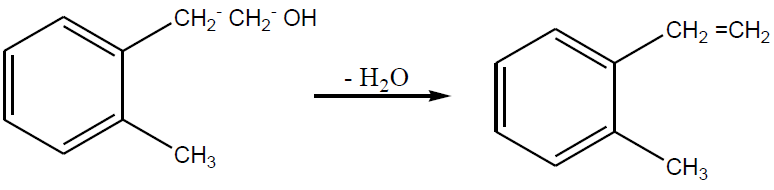
3.4.
Exercice 4
I-1 Procédé : le procédé de contact a remplacé ces dernières décennies le procédé traditionnel de la chambre de plomb datant du $18eme$ siècle.
Equations:
$SO_{2} + O_{2}\longrightarrow SO_{3}$
$SO_{3} + H_{2}O H_{2}SO_{4}$
I.2 Utilisations : l’acide sulfurique sert essentiellement à la fabrication d’engrais.
Il est également utilisé pour la production de textiles, le traitement de minerais, le raffinage du pétrole, le stockage de l’électricité dans les batteries au plomb, le décapage des métaux et la synthèse de colorants, explosifs, détergents etc.

Ajouter un commentaire