Corrigé BFEM Physique chimie 2016
Exercice 1
1) Déterminons la concentration massique
On a : $c_{m}=\dfrac{m}{V}\ $ avec $\ m=n\times M$
Donc, $c_{m}=\dfrac{n\times M}{V}\ $ or $\ \dfrac{n}{V}=c$
D'où, $c_{m}=c\times M\ $ avec $M_{(HCl)}=1+35.5=36.5\;g.mol^{-1}$
A.N : $c_{m}=2\;10^{-1}\times 36.5=7.3$
Donc, $$\boxed{c_{m}=7.3\;g.l^{-1}}$$
2) Calculons la concentration molaire de $NaOH$
Soit $A$ la solution de $HCl$ et $B$ la solution de $NaOH$
A l'équivalence on a : $n_{A}=n_{B}\ $ or $n=c\times V$
Donc, $c_{A}V_{A}=c_{B}V_{B}$
D'où, $c_{B}=\dfrac{c_{A}V_{A}}{V_{B}}$
A.N : $c_{B}=\dfrac{2\;10^{-1}\times 80}{40}=0.4$
Donc, $$\boxed{c_{B}=0.4\;mol.l^{-1}}$$
3) On verse $120\;ml$ de $HCl$ dans du zinc.
3) 1) Écrivons l'équation bilan. On a : $$2HCl\ +\ Zn \longrightarrow\ ZnCl_{2}\ +\ H_{2}$$
3) 2) Trouvons le volume de $H_{2}$ dégagé.
On a du $Zn$ en excès, donc toute la quantité de $HCl$ a réagi.
D'après l'équation ci-dessus, on a : $\dfrac{n_{(HCl)}}{2}=\dfrac{n_{(H_{2})}}{1}$
Donc, $n_{(HCl)}=2n_{(H_{2})}\ $ or $\ n=cV=\dfrac{V}{V_{M}}$
Ainsi, $c_{(HCl)}V_{(HCl)}=2\dfrac{V_{(H_{2})}}{V_{M}}$
D'où, $V_{(H_{2})}=\dfrac{c_{(HCl)}\times V_{(HCl)}\times V_{M}}{2}$
A.N : $V_{(H_{2})}=\dfrac{2\;10^{-1}\times 120\;10^{-3}\times 22.4}{2}=0.2688$
Donc, $$\boxed{V_{(H_{2})}=268.8\;ml}$$
Exercice 2
1) Le méthane appartient à la famille des alcanes.
2) Écrivons la formule générale de cette famille.
Soit un alcane $A$ de $n$ atomes de carbones, alors $A$ est de la forme $$C_{n}H_{2n+2}$$
3) Équation bilan complète de la combustion complète du méthane.
$$CH_{4}\ +\ 2O_{2} \longrightarrow\ CO_{2}\ +\ 2H_{2}O$$
4) Calculons le volume de $O_{2}$ nécessaire.
D'après l'équation bilan on a :
$\dfrac{n_{(CH_{4})}}{1}=\dfrac{n_{(O_{2})}}{2}$ or $n=\dfrac{m}{M}=\dfrac{V}{V_{M}}$
Donc, $\dfrac{m_{(CH_{4})}}{M_{(CH_{4})}}=\dfrac{V_{(O_{2})}}{2V_{M}}\ $ or $M_{(CH_{4})}=12+4=16\;g.mol^{-1}$
Alors on aura : $V_{(O_{2})}=\dfrac{m_{(CH_{4})}\times 2V_{M}}{M_{(CH_{4})}}$
A.N : $V_{(O_{2})}=\dfrac{320\times 2\times 24}{16}=960$
Donc, $$\boxed{V_{(O_{2})}=960\;l}$$
5) Trouvons la masse de $CO_{2}$ formée.
D'après l'équation bilan de la question 3) on a :
$\dfrac{n_{(CH_{4})}}{1}=\dfrac{n_{(CO_{2})}}{1}$ or $n=\dfrac{m}{M}$
Donc, $\dfrac{m_{(CH_{4})}}{M_{(CH_{4})}}=\dfrac{m_{(CO_{2})}}{M_{(CO_{2})}}\ $ avec $M_{(CH_{4})}=16\;g.mol^{-1}$ et $M_{(CO_{2})}=12+2\times 16=44\;g.mol^{-1}$
Alors on aura : $m_{(CO_{2})}=\dfrac{m_{(CH_{4})}\times M_{(CO_{2})}}{M_{(CH_{4})}}$
A.N : $m_{(CO_{2})}=\dfrac{320\times 44}{16}=880$
Donc, $$\boxed{m_{(CO_{2})}=880\;g}$$
Exercice 3
1) Calculons la distance focale
On a : $v=\dfrac{1}{f}$, donc $f=\dfrac{1}{v}$
A.N : $f=\dfrac{1}{40}=0.025$
Donc, $$\boxed{f=2.5\;cm}$$
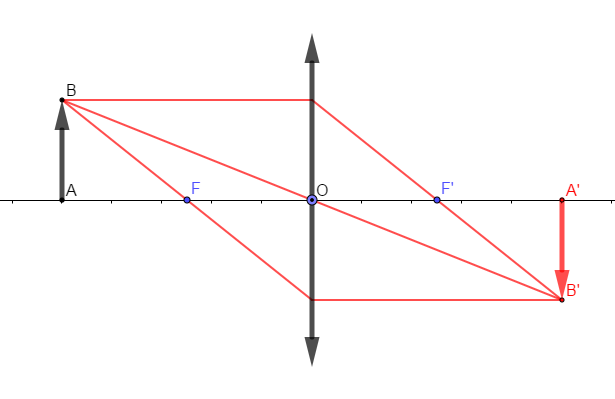
2) Construisons l'image $A'B'$ de l'objet $AB$

3) Déterminons :
$-\ $ la hauteur $A'B'$
On a : $A'B'=2\;cm$
$-\ $ la distance $OA$
On a : $OA=5\;cm$
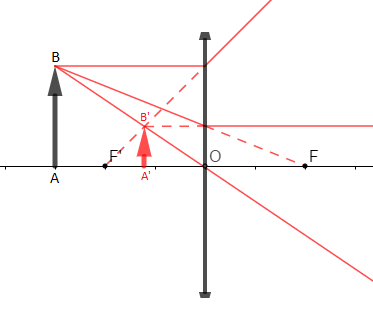
4) Construisons l'image de ce même objet par une lentille divergente.

Exercice 4
1) Énonçons la loi de Joule
La quantité de chaleur dégagée dans un conducteur par le passage d'un courant électrique est :
$-\ $ proportionnelle au temps $t$ de passage du courant.
$-\ $ proportionnelle au carré de l'intensité $I$ du courant.
$-\ $ variable avec la résistance $R$ du conducteur.
On a : $E=W=R.I^{2}.t$
2) Calculons $R_{1}$
D'après la loi de Joule on a : $E=R_{1}I^{2}t$
Alors, $R_{1}=\dfrac{E}{I^{2}t}$
A.N : $R_{1}=\dfrac{60\;10^{3}}{2^{2}\times 5\times 60}=50$
Donc, $$\boxed{R_{1}=50\;\Omega}$$
3) Calculons la tension $U$
On a : $U=R_{1}I$
A.N : $U=50\times 2=100$
Donc, $$\boxed{U=100\;V}$$
4) 1) Les conducteurs de résistances $R_{1}$ et $R_{2}$ sont montés en parallèles car la résistance équivalente est inférieure à $R_{1}.$
Par ailleurs, si les conducteurs étaient montés en série, alors la résistance équivalente $(R_{eq}=R_{1}+R_{2})$ serait supérieure à $R_{1}.$
4) 2) Calculons $R_{2}$
On a : $\dfrac{1}{R_{eq}}=\dfrac{1}{R_{1}}+\dfrac{1}{R_{2}}$
alors on aura : $\dfrac{1}{R_{2}}=\dfrac{1}{R_{eq}}-\dfrac{1}{R_{1}}=\dfrac{R_{1}-R_{eq}}{R_{eq}R_{1}}$
donc, $R_{2}=\dfrac{R_{eq}R_{1}}{R_{1}-R_{eq}}$
A.N : $R_{1}=\dfrac{50\times 20}{50-20}=33.333$
Ainsi, $$\boxed{R_{2}=33.333\;\Omega}$$
Auteur:
Aliou ndiaye

Commentaires
Assane (non vérifié)
dim, 05/05/2019 - 14:51
Permalien
Site pédagogique très utile
Anonyme (non vérifié)
mar, 07/16/2019 - 21:09
Permalien
C'est bon pour moi
Anonyme (non vérifié)
mar, 05/26/2020 - 02:33
Permalien
excusez moi mais je pense qu
fdini
mar, 05/26/2020 - 05:38
Permalien
merci pour le retour, ct une
merci pour le retour, ct une faute de frappe mais on l'a corrigé
Anonyme (non vérifié)
ven, 07/09/2021 - 06:10
Permalien
Au niveau de l'exercice 1on
Anonyme (non vérifié)
ven, 07/16/2021 - 23:40
Permalien
C'est bien ça35,5+1=36,5
Moustephe (non vérifié)
jeu, 08/05/2021 - 13:27
Permalien
Au niveau de l'éxo 2 vous n
Ajouter un commentaire