Exercices sur les hydrocarbures 3e
Classe:
Troisième
Exercice 1
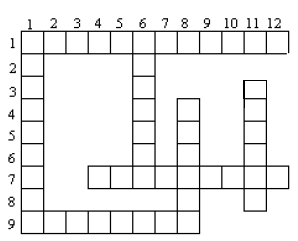
Indiquer les mots permettant de remplir la grille
Horizontalement :
1 : corps organiques constitués de carbone et d'hydrogène
7 : premier hydrocarbure de la famille des alcynes
9 : sa formule chimique est $C_{2}H_{4}$
Verticalement :
1 : un des constituants des hydrocarbures
7 : sa combustion complète donne du dioxyde de carbone
8 : hydrocarbures de formule générale $C_{n}H_{2n-2}$
11 : hydrocarbure sature de masse molaire $58\; g.mol^{-1}$
Exercice 2
Équilibrer chacune des équations chimiques générales suivantes
1) $C_{n}H_{2n+1}\ +\ O_{2}\longrightarrow\ CO_{2}\ +\ H_{2}O$
2) $C_{n}H_{2n}\ +\ O_{2}\longrightarrow\ CO_{2}\ +\ H_{2}O$
3) $C_{n}H_{2n-2}\ +\ O_{2}\longrightarrow\ CO_{2}\ +\ H_{2}O$
Exercice 3
Quels sont, parmi les corps suivants, ceux qui sont des hydrocarbures ?
$C_{2}H_{4}$ éthylène ; $C_{2}H_{6}O$ alcool ; $C_{2}H_{2}$ acétylène ; $C_{6}H_{6}$ benzène ; $CS_{2}$ sulfure de carbone ; $C_{5}H_{12}$ pentane ; $H_{2}S$ sulfure d'hydrogène.
Exercice 4
Donner la formule chimique :
1) d'un alcane dont la molécule renferme 6 atomes de carbone
2) d'un alcène dont la molécule renferme 8 atomes d'hydrogène
3) d'un alcyne dont la molécule renferme 5 atomes de carbone.
Exercice 5
L'analyse d'un hydrocarbure a permis de noter que sa molécule renferme huit (8) atomes d'hydrogène et de masse molaire $80\;g/mol$.
1) Trouver la formule chimique de cet hydrocarbure.
2) Calculer le volume de dioxyde de carbone que l'on obtient dans les conditions normales en faisant la combustion complète de $20.5\;g$ de cet hydrocarbure.
3) Un alcane a une masse molaire de $72\;g/mol$, donner sa formule chimique.
Exercice 6
On brûle $17\;cm^{3}$ d'un alcane gazeux dans un excès de dioxygène. Après cette combustion complète, il s'est formé $68\;cm^{3}$ de dioxyde de carbone. Trouver la formule brute de l'alcane brûlé.
Exercice 7
Une bouteille de butagaz contient $13\;kg$ de butane $C_{4}H_{10}$.
1) Écrire l'équation bilan de la combustion complète du butane
2) Trouver le volume de dioxygène, mesuré dans les conditions normales, nécessaire pour assurer cette combustion. En déduire le volume d'air nécessaire.
Exercice 8
Dans le kérosène, carburant des avions à réaction, on trouve un hydrocarbure de formule $C_{12}H_{26}$ que l'on appelle le duodécane ; à quelle famille d'hydrocarbure appartient-il ?
Quelle masse minimale de dioxygène faut-il prévoir pour brûler les 600 tonnes de kérosène que contient le premier étage de la fusée Saturne V, lanceur du programme Apollo.
Exercice 9
On introduit dans un tube appelé eudiomètre, $10\;cm^{3}$ d'un hydrocarbure gazeux $A$ et $80\;cm^{3}$ de dioxygène. On fait jaillir une étincelle qui déclenche la combustion complète du mélange. Après refroidissement, il reste dans l'eudiomètre un mélange gazeux dont l'analyse révèle qu'il est constitué de $40\;cm^{3}$ de dioxyde de carbone et $20\;cm^{3}$ de dioxygène. Le volume molaire dans les conditions normales est $V_{m}=22.4\;L/mol.$
1) Écris l'équation bilan de la combustion complète du composé $A.$
2) Détermine le volume de dioxygène réagi et le volume de dioxyde de carbone formé.
3) Déduis en la formule brute du composé $A.$
Activités
Masses molaires atomiques :
$M(H)=1g\cdot mol^{-1}$ ; $M(C)=12g\cdot mol^{-1}$ ; $M(O)=16g\cdot mol^{-1}$
Volume molaire des gaz dans les conditions expérimentales :
$V_{M}=24L\cdot mol^{-1}$
Décris des expériences à faire pour montrer que, lors de la combustion du butane (briquet), il se forme de l'eau et du dioxyde de carbone.
Exercice 10 Contrôle de connaissances
Compléter les phrases ci-dessous.
1) Les hydrocarbures sont des composés ne contenant que les éléments .......... et ................
Les alcanes ont pour formule générale ...............
2) Les alcènes ont pour formule générale ..............
3) L'acétylène de formule $C_{2}H_{2}$ est un hydrocarbure appartenant à la famille des ................
4) La combustion complète d'un hydrocarbure dans le dioxygène donne ............. et de ..............
5) Si la combustion est ............., il se forme entre autres des fumées noires de carbone.
Exercice 11 Identifier la famille à laquelle appartient un hydrocarbure à partir de sa formule brute.
1) Définis un hydrocarbure
2) Cite trois familles d'hydrocarbures et préciser leurs formules générales
3) Parmi les corps suivants, lesquels sont des hydrocarbures ;
Préciser leur famille.
$C_{3}H_{4}$ ; $CO_{2}$ ; $NH_{3}$ ; $H_{2}O$ ; $C_{2}H_{2}$ ; $O_{2}$ ; $CH_{4}$
Exercice 12 Identifier un hydrocarbure à partir de sa masse molaire
1) Identifier un alcane
a) Déterminer l'expression de la masse molaire moléculaire d'un alcane possédant $n$ atomes de carbone.
b) Déduis-en la formule brute d'un alcane dont la masse molaire est $M=30g\cdot mol^{-1}.$
2) Identifier un alcène
a) Déterminer l'expression de la masse molaire moléculaire d'un alcène possédant $n$ atomes de carbone
b) Déduis-en la formule brute d'un alcène dont la masse molaire est $M=28g\cdot mol^{-1}.$
3) Identifier un alcène
a) Déterminer l'expression de la masse molaire moléculaire d'un alcyne possédant $n$ atomes de carbone.
b) Déduis-en la formule brute d'un alcène dont la masse molaire est $M=26g\cdot mol^{-1}.$
4) La densité d'un alcane gazeux est $2$
a) Rappelle la formule de la densité d'un gaz par rapport à l'air.
b) Trouve la formule brute de l'alcane.
Exercice 13 Équation-bilan de la combustion complète d'un hydrocarbure
Complète et équilibre les équations
$C_{3}H_{8}\ +\ \ldots\ \rightarrow\ CO_{2}\ +\ H_{2}O$
$C_{2}H_{4}\ +\ O_{2}\ \rightarrow\ CO_{2}\ +\ \ldots$
$C_{2}H_{2}\ +\ O_{2}\ \rightarrow\ H_{2}O\ +\ \ldots$
$C_{4}H_{10}\ +\ O_{2}\ \rightarrow\ CO_{2}\ +\ H_{2}O$
Exercice 14 Utiliser l'équation bilan de la combustion complète d'un hydrocarbure
Le méthane $CH_{4}$ brûle dans le dioxygène $O_{2}$ en donnant du dioxyde de carbone $CO_{2}$ et de l'eau $H_{2}O$
1) Écris l'équation bilan de la réaction
2) Donne l'interprétation du bilan en mole
3) On dispose de $3$ mol de méthane
a) Quelle quantité de matière de dioxygène faut-il pour que la combustion soit complète.
b) Calcule le volume de dioxyde de carbone et la masse d'eau formés
Exercice 15 Du gaz à la cuisine
Un alcane $A$ est utilisé comme gaz de cuisine
La masse molaire moléculaire de $A$ est de $M=58g\cdot mol^{-1}.$
1) Rappelle la formule générale des alcanes en fonction du $n$ d'atomes de carbone.
2) Trouve la formule brute de l'alcane $A$ et donner son nom.
3) La combustion complète d'une masse m de l'alcane $A$ produit $4$ moles de dioxyde de carbone.
a) Écris l'équation-bilan de la réaction.
b) Trouve la masse $m$ d'alcane utilisée.
Exercice 16 soudure métallique
La combustion complète de l'acétylène produit une quantité de chaleur qui permet d'atteindre des températures élevées.
Cette combustion est utilisée dans le chalumeau oxyacétylénique pour effectuer des soudures métalliques
L'acétylène encore appelé éthyne, a pour formule brute $C_{2}H_{2}$
1) A quelle famille d'hydrocarbure appartient l'acétylène ?
2) Écris la formule générale des hydrocarbures de cette famille
3) Écris l'équation bilan de la combustion complète de l'acétylène dans le dioxygène.
4) On brule complètement 48L de gaz acétylène dans l'air
a) Calculer le volume de dioxygène nécessaire pour cette combustion.
b) Quel est le volume d'air utilisé sachant que l'air renferme en volume $\dfrac{1}{5}$ de dioxygène
Exercice supplémentaire Exclusif document.
Mort des enfants de la famille [...] aux Parcelles assainies :
Les résultats de l'autopsie.
Le certificat de genre de mort est sans ambages.
Il a révélé que les cinq enfants de la famille [...] de l'Unité $17$ des Parcelles Assainies sont morts par asphyxie après avoir inhalé de la fumée provenant d'un incendie.
Source : un journal dakarois publié le $13$ mai $2017.$
En effet tous les ans, au Sénégal, surtout en période de fraicheur, des personnes s'intoxiquent en brûlant du charbon dans des fourneaux comme l'indique la photo ci-dessous.

1) Indique le gaz responsable de cette intoxication.
2) Explique comment il est produit.
3) Propose une action que l'on doit faire pour éviter le risque d'intoxication.
$\begin{array}{c}\blacktriangleright\,\boxed{\text{Correction des exercices}}\end{array}$
Source:
irempt.ucad.sn & ADEM

Commentaires
Marcel Badji (non vérifié)
dim, 10/21/2018 - 15:58
Permalien
Vous pouvez me donner les corrections s'il vous plait
Baye LAT DIOUF (non vérifié)
dim, 10/21/2018 - 21:55
Permalien
Je voudrais voir la
Mouanda Jeannie (non vérifié)
jeu, 04/09/2020 - 23:44
Permalien
Apprendre
Mareme diop (non vérifié)
mar, 01/12/2021 - 22:12
Permalien
Conprendre
Mareme diop (non vérifié)
dim, 01/17/2021 - 15:26
Permalien
Comprendre
Akim (non vérifié)
mer, 01/27/2021 - 22:59
Permalien
Correction
Serge (non vérifié)
dim, 01/02/2022 - 17:23
Permalien
Déterminer le volume de dioxygene nécessaire pour réaliser la co
Antou (non vérifié)
mar, 07/12/2022 - 17:05
Permalien
Apprendre
Lamine diallo (non vérifié)
mer, 10/26/2022 - 00:29
Permalien
Exercise 15 correcting
Nafissatou nden... (non vérifié)
lun, 11/14/2022 - 21:46
Permalien
Corriger
Mane (non vérifié)
mer, 03/27/2019 - 15:44
Permalien
Avoir la correction
Bouanga (non vérifié)
lun, 11/25/2019 - 22:35
Permalien
comprendre la physique
Aminata Mouhamed Ly (non vérifié)
mar, 02/02/2021 - 21:22
Permalien
correction de l'exercice 5
Anonyme (non vérifié)
mar, 02/02/2021 - 21:24
Permalien
avoir la correction de l
Modou (non vérifié)
lun, 07/20/2020 - 23:09
Permalien
Avoir la correction des exercices
Hassanatou Cher... (non vérifié)
ven, 08/07/2020 - 17:55
Permalien
Corrigé de l'exercice
Astou (non vérifié)
lun, 01/25/2021 - 22:43
Permalien
Hydrocarbures
Mamadou Ndiaye DIOP (non vérifié)
jeu, 12/17/2020 - 19:25
Permalien
voit la correction
Mamadou Ndiaye DIOP (non vérifié)
dim, 12/20/2020 - 01:38
Permalien
Voir les corrections
Mamadou Ndiaye DIOP (non vérifié)
dim, 12/20/2020 - 01:41
Permalien
Voir les corrections
Mamadou Ndiaye DIOP (non vérifié)
dim, 12/20/2020 - 01:45
Permalien
Voir les corrections
Sidibé (non vérifié)
mer, 06/16/2021 - 13:03
Permalien
Je suis élève de 3eme
Sidibé (non vérifié)
mer, 06/16/2021 - 13:04
Permalien
Je suis élève de 3eme
Anonyme (non vérifié)
jeu, 11/10/2022 - 19:58
Permalien
hehehe c est pour les prof
Mbene Diallo (non vérifié)
mer, 12/13/2023 - 20:47
Permalien
Exercice
Baye bame (non vérifié)
mer, 06/01/2022 - 16:09
Permalien
je ne veux l'exercice 15 et 16
Mouhamed (non vérifié)
mar, 02/06/2024 - 22:13
Permalien
Correction exercice 5
isseu (non vérifié)
jeu, 07/22/2021 - 23:00
Permalien
je veux voir la correction
Fatima Zahra dieng (non vérifié)
mer, 11/24/2021 - 20:26
Permalien
Demande d'informations
Fatima Zahra dieng (non vérifié)
mer, 11/24/2021 - 20:26
Permalien
Demande d'informations
Ndeye seye (non vérifié)
dim, 11/27/2022 - 20:23
Permalien
Voir les corrections
Mariame sakho (non vérifié)
jeu, 11/09/2023 - 23:22
Permalien
Réviser
Marista diallo (non vérifié)
ven, 06/10/2022 - 19:12
Permalien
Apprendre
AICHA (non vérifié)
dim, 07/03/2022 - 01:47
Permalien
Exo16
AICHA (non vérifié)
dim, 07/03/2022 - 01:47
Permalien
Exo16
Thier (non vérifié)
mar, 11/15/2022 - 21:42
Permalien
Mieux comprendre
Mombo (non vérifié)
lun, 01/30/2023 - 15:41
Permalien
Corrigé
Maurina ékoga (non vérifié)
jeu, 01/18/2024 - 15:28
Permalien
Correction
X (non vérifié)
dim, 11/10/2024 - 13:08
Permalien
Demande de correction
FKS (non vérifié)
dim, 10/28/2018 - 18:52
Permalien
Pouvez vous revoir l'exo 5
Ndiaye (non vérifié)
sam, 01/05/2019 - 13:25
Permalien
Réussir
Diallo (non vérifié)
sam, 03/30/2019 - 12:41
Permalien
Reissue BFEM
ndèye awa (non vérifié)
sam, 06/01/2019 - 01:03
Permalien
rwusair le bfeem
TRA BI JEAN FRANÇOIS (non vérifié)
mer, 10/31/2018 - 10:50
Permalien
Aidez moi
mndiaye
lun, 11/12/2018 - 10:14
Permalien
Vous avez la solution de
Vous avez la solution de votre exercice sur ce lien.
http://www.sunudaara.com/physique_chimie/solutions-des-exercices-les-hyd...
koudite (non vérifié)
jeu, 11/01/2018 - 11:40
Permalien
etudier
Aminata sall (non vérifié)
lun, 11/12/2018 - 00:08
Permalien
Correction s’il Vous plaît
mndiaye
lun, 11/12/2018 - 11:07
Permalien
On travaille sur la
On travaille sur la correction des exercices. Vous l'aurez bientôt en ligne.
Mbene Diallo (non vérifié)
mer, 12/13/2023 - 20:48
Permalien
Exercice
Samou (non vérifié)
mar, 11/27/2018 - 17:53
Permalien
Des exercice
Pages
Ajouter un commentaire