Exercices sur la calorimétrie 3e
Classe:
Troisième
Exercice 1
On prélève $300\;g$ d'eau à $20^{o}\;C$ que l'on porte à l'ébullition ; quelle quantité de chaleur a-t-on fournie à cette eau ?
Exercice 2
Pour chauffer $250\;g$ d'huile à $70^{o}\;C$, on lui fournit $20 000\;J$. Sa température varie alors de $40^{o}\;C$. Trouver :
1) La chaleur massique de cette huile.
2) Sa température initiale
Exercice 3
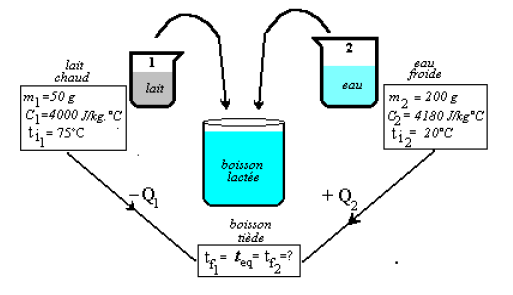
Pour obtenir une boisson lactée tiède, Mactar réalise le mélange schématisé ci-contre. Trouver :
1) La quantité de chaleur perdue par le lait chaud
2) La quantité de chaleur reçue par l'eau froide
3) la température de sa boisson lactée tiède
Exercice 4
Dans un récipient contenant $400\;g$ d'eau à $25^{o}\;C$, on ajoute $100\;g$ d'eau à $75^{o}\;C$. Quelle est, en l'absence de toute perte de chaleur, la température finale du mélange obtenue ?
Exercice 5
Situation - problème
Sachant que les chaleurs massiques respectives de l'eau et du jus sont : $4180\;J/kg^{o}\;C$ et $2090\;J/kg^{o}\;C$ et que la valeur en eau du calorimètre est $20\;g$ trouver :
1) La quantité de chaleur perdue par les corps chauds.
2) La quantité de chaleur reçue par les corps froids
3) Quelle est alors la température de la tisane obtenue ?
Exercice 6
On a mélangé une masse $m_{1}$ d'eau chaude à la température $t_{1}=80^{o}\;C$ et une masse $m_{2}$ d'eau froide à la température $t_{2}=20^{o}\;C$. On a ainsi obtenu une masse d'eau totale de $1200\;g$ d'eau à la température $t=30^{o}\;C$.
Écrire l'expression de la quantité de chaleur perdue par l'eau chaleur et l'expression de la quantité de chaleur reçue par l'eau froide. Quelles étaient les valeurs des masses $m_{1}$ et $m_{2}$ ?
On veut porter les $1200\;g$ d'eau de $30^{o}\;C$ à $50^{o}\;C$ au moyen d'une résistance $R=20\;\Omega$ traversé par un courant d'intensité $I=5\;A$. Pendant quelle durée, doit-on faire passer le courant dans $R$ si on admet que toute la chaleur produite par effet - Joule sert à chauffer l'eau
$\begin{array}{c}\blacktriangleright\,\boxed{\text{Correction des exercices}}\end{array}$
Source:
irempt.ucad.sn

Commentaires
BOUBOU dioum (non vérifié)
dim, 07/25/2021 - 22:41
Permalien
Pc
Ajouter un commentaire