Solution des exercice : Généralité sur la chimie organique - 1L
Classe:
Première
Exercice 1
Mots croisés

Exercice 2
Choisissons la bonne réponse
1. La liaison covalente provient de :
a. la mise en commun de deux électrons célibataires par deux atomes ;
2. On définit les isomères chimiques comme :
a. des espèces chimiques de même formule brute mais qui diffèrent par leurs structures.
3. En chimie organique, les isomères, qui existent, sont:
b. trois types (squelette, position et fonction) ;
4. L'analyse élémentaire quantitative d'une substance permet de déterminer :
c. le nombre de môle d'atomes de chaque élément contenu dans cette substance.
5. La somme des masses des éléments constitutifs d'un échantillon d'une substance est:
c. égale à la masse de l'échantillon analysé aux erreurs d'expérience près.
6. Pour déterminer la formule brute d'une substance il suffit de connaître :
c. la masse molaire et les résultats de l'analyse élémentaires qualitative et quantitative de la substance
Exercice 3
Complétons ce texte avec les mots ou groupe de mots suivants : oxydes de carbone ; organique ; biologique ; chimie ; minérale ; carbone ;combustibles ; chimie organique ; caractère minéral ; végétale ; animal ; carbures.
A l'origine, la chimie organique étudiait les substances des êtres vivants appartenant au monde animal ou végétal.
Elle s'opposait à la chimie minérale (chimie inorganique) qui se consacrait aux substances extraites du monde minéral, c'est-à-dire provenant des roches, des eaux naturelles, de l'atmosphère.
Ce n'est qu'en 1828 Wöhler (chimiste allemand) réussit à créer l'urée substance biologique à partir d'un composé minéral$\ldots$
On comprit alors que la chimie organique obéissait aux mêmes règles que la chimie minérale
Mais la distinction demeure en raison entre autres des propriétés particulières des composés organiques par rapport aux composés minéraux. Ainsi les composés organiques (pétroles, gaz naturel, alcool...) sont presque combustibles, ce qui est rarement le cas des composés minéraux
La chimie organique est la chimie des composés du carbone.
Certains sont d'origine naturelle, animale ou végétale d'où l'appellation "organique" (s'oppose à la chimie minérale).
Les médicaments, matières plastiques, fibres synthétiques, peintures, additifs alimentaires sont des produits de la chimie organique obtenus par synthèse, c'est à dire par formation d'une molécule à partir de molécules plus simples.
En fait il faut en exclure le carbone, les oxydes de carbone, les carbonates, les cyanures les carbures qui ont tous un caractère minéral
Exercice 4
Lire attentivement ce texte avant de répondre aux questions
En $1800$, la chimie s'était fermement établie parmi les sciences ; au cours de la décennie suivante, les scientifiques se sont vivement intéressés à l'étude de la composition des substances et à la manière don telles pouvaient être modifiées.
Par suite de recherches, ils ont commencé à faire la distinction entre deux genres de composés : ceux qui étaient issus de sources végétales ou animales on tété appelés composés organiques, et ceux qui provenaient de constituants minéraux de la Terre ont été appelés « inorganiques ».
Les chimistes connaissaient l'existence de très nombreux composés organiques telles que les teintures, les savons, le vinaigre, le sucre, les parfums, les gommes et le caoutchouc, pour n'en mentionner que quelques-uns, mais ils n'arrivaient pas à expliquer comment tant de composés pouvaient être faits à partir de quelques éléments seulement...()
Jusqu'alors, on n' avait jamais synthétisé un composé organique à partir de matières inorganiques; par conséquent, de nombreux scientifiques croyaient que les composés organiques se formaient sous l'influence d'une « force vitale ».
En $1828$, Friedrich Wöhler a fait une découverte remarquable.
Il a essayé de fabriquer du cyanate d'ammonium au moyen d'une réaction de décomposition double, dans une solution de chlorure d'ammonium et de cyanate d'argent.
Or, ces deux composés étaient considérés comme étant « inorganiques ».
Cependant, au lieu d'obtenir du cyanate d'ammonium, il a produit des cristaux d'urée, un composé organique
Au cours des années qui ont suivi cette découverte et après que l'acide acétique et plusieurs autres composés organiques eurent été fabriqués à partir de matières inorganiques, la validité de la « force vitale » a été mise en doute.
Avec le temps, de plus en plus de composés organiques ont été synthétisés à partir de matières inorganiques.
Il est devenu évident qu'il n'était pas nécessaire que tous les composés organiques soient associés à des organismes vivants.
Au milieu des années $1850$, on a compris que le facteur commun à tous les composés organiques était le carbone.
Maintenant, les chimistes disent simplement que les composés organiques sont ceux qui contiennent du carbone, sauf les oxydes de carbone, les carbonates,les carbures et les cyanures.
Ces exceptions, en plus de toutes les autres substances connues,sont dites inorganiques.
Trois à quatre millions de composés organiques sont connus tandis que seulement cinquante mille composés inorganiques sont connus
1. Donner un titre à ce texte
2. Le texte fait allusion au premier composé organique fabriqué.
Lequel ?
Et quels sont les composés minéraux utilisés pour cette synthèse
2. Citer les composés organiques et les composés minéraux
3. Quelle est la chimie qui s'opposait à la chimie organique ?
2. Définir la chimie organique
Exercice 5
Classons ces composés en composées minéraux ou organique
$$\begin{array}{|l|l|} \hline \text{Composés minéraux}&\text{Composés organiques}\\ \hline CO_{2}\ ;\ CO\ ;\ CaCO_{3}\ ;\ HCN& CH_{4}\ ;\ C_{2}H_{2}\ ;\ C_{2}H_{6}\ ;\ C_{2}H_{4}\\ CaCO_{3}\ ;\ CH_{4}ON_{2}\ ;\ HNO_{3}&C_{3}H_{6}\ ;\ C_{5}H_{12}\ ;\ C_{55}H_{72}N_{4}O_{5}Mg\\ &CH_{4}ON_{2}\ .\ CH_{3}Cl\\\hline \end{array}$$
Exercice 6
La donnée qui permet de distinguer ces quatre composés est
1. La masse atomique relative des éléments
Exercice 7
1. La masse molaire moléculaire de l'acide acétique
$\begin{array}{lll} M_{C_{2}H_{4}O_{2}}&=&2M_{C}+4M_{H}+2M_{O}\\\\&=&2\times 12+4\times 1+2\times 16\\\\\Rightarrow\;M_{C_{2}H_{4}O_{2}}&=&60\,g\cdot mol^{-1} \end{array}$
2. Détermination des pourcentages en masse de chaque élément présent dans ce composé.
$\begin{array}{lll}\%C&=&\dfrac{2M_{C}\times 100}{M_{C_{2}H_{4}O_{2}}}\\\\&=&\dfrac{2\times 12.0\times 100}{60}\\\\\Rightarrow\%C&=&40.0\%\end{array}$
$\begin{array}{lll}\%H&=&\dfrac{4M_{H}\times 100}{M_{C_{2}H_{4}O_{2}}}\\\\&=&\dfrac{4\times 1.0\times 100}{60}\\\\\Rightarrow\%H&=&6.70\%\end{array}$
$\begin{array}{lll}\%O&=&\dfrac{2M_{O}\times 100}{M_{C_{2}H_{4}O_{2}}}\\\\&=&\dfrac{2\times 16.0\times 100}{60}\\\\\Rightarrow\%O&=&53.3\%\end{array}$
Exercice 8
1. Calcul du pourcentage massique de magnésium contenu dans la chlorophylle
$\begin{array}{lll}\%Mg&=&\dfrac{M_{Mg}\times 100}{M_{C_{55}H_{72}N_{4}O_{5}Mg}}\\\\&=&\dfrac{24\times 100}{(55\times 12+72\times 1.00+4\times 14+5\times 16+24)}\\\\\Rightarrow\%Mg&=&2.69\%\end{array}$
2. Calcule de la masse de magnésium absorbée lorsqu'on mange $100\,g$ de feuilles Masse de cholophylle contenue dans $100\,g$ de feuilles
$m=\dfrac{100\times 1}{0.5}\Rightarrow\;m=200\,g$
$\begin{array}{lll}m_{Mg}&=&\%Mg\times m\\\\\Rightarrow\;m_{Mg}&=&\dfrac{2.69}{100}\times 200\,g\\\\\Rightarrow\;m_{Mg}&=&5.38\,g\end{array}$
3. Le nombre correspondant d'atomes de magnésium
$\begin{array}{lll}N&=&nN_{A}\\\\&=&\dfrac{m_{Mg}}{M_{Mg}}N_{A}\\\\&=&\dfrac{5.38}{24}\times 6.02\cdot 10^{23}\\\\\Rightarrow\;N&=&1.35\cdot 10^{23}\text{atomes}\end{array}$
Exercice 9
1. Calcul de la masse de molaire de ce composé
$M=29d=29\times 3.03\Rightarrow\;M=87.87\,g\cdot mol^{-1}$
2. Détermination de sa formule brute :
Soit $C_{x}H_{y}O_{z}$ la formule brute du composé
$\begin{array}{lll}\%C&=&\dfrac{xM_{C}\times 100}{M_{C_{x}H_{y}O_{z}}}\\\\&=&\dfrac{12x\times 100}{M_{C_{x}H_{y}O_{z}}}\\\\\Rightarrow\;x&=&\dfrac{\%C\times M_{C_{x}H_{y}O_{z}}}{12\times 100}\\\\&=&\dfrac{54.5\times 87.87}{12\times 100}\\\\\Rightarrow\;x&=&4\end{array}$
$\begin{array}{lll}y&=&\dfrac{\%H\times M_{C_{x}H_{y}O_{z}}}{1\times100}\\\\&=&\dfrac{9.1\times 87.87}{1\times 100}\\\\\Rightarrow\;y&=&8\end{array}$
$\begin{array}{lll}z&=&\dfrac{\%O\times M_{C_{x}H_{y}O_{z}}}{16\times100}\\\\&=&\dfrac{36.4\times 87.87}{16\times 100}\\\\\Rightarrow\;z&=&2\end{array}$
$\Rightarrow\;C_{4}H_{8}O_{2}$
3.1 Équation bilan de la réaction chimique
$C_{4}H_{8}O_{2}\ +\ 5O_{2}\ \longrightarrow 4CO_{2}\ +\ 4H_{2}O$
3.2. Calcul du volume de dioxygène nécessaire pour que la combustion soit complète.
Nombre de moles du composé $A$
$\begin{array}{lll}n_{A}&=&\dfrac{m_{A}}{M_{A}}\\&=&\dfrac{3.4}{87.87}\\\Rightarrow\;n_{A}&=&0.039\,mol\end{array}$
$\begin{array}{lll}n_{O_{2}}&=&5_{n_{A}}\\&=&5\times 0.039\\\Rightarrow\;n_{O_{2}}&=&0.195mol\\\Rightarrow\;V_{O_{2}}&=&n_{O_{2}}\times V_{m}\\&=&0.195\times 22.4\\\Rightarrow\;V_{O_{2}}&=&4.37L\end{array}$
Exercice 10
Choisissons, parmi les formules moléculaires suivantes, celle en accord avec cette composition.
Déterminons le pourcentage de carbone contenu dans chaque composé
$\begin{array}{lll}\%C&=&\dfrac{6M_{C}\times 100}{M_{C_{6}H_{14}O_{2}}}\\\\&=&\dfrac{6\times 12\times 100}{(6\times 12+1\times 14+2\times 16)}\\\\\Rightarrow\%C&=&16\end{array}$
$\begin{array}{lll}\%C&=&\dfrac{6M_{C}\times 100}{M_{C_{6}H_{10}}}\\\\&=&\dfrac{6\times 12\times 100}{(6\times 12+1\times 10)}\\\\\Rightarrow\%C&=&87.8\end{array}$
$\begin{array}{lll}\%C&=&\dfrac{M_{C}\times 100}{M_{CH_{4}O}}\\\\&=&\dfrac{12\times 100}{(1\times 12+1\times 4+16)}\\\\\Rightarrow\%C&=&37.5\end{array}$
$\begin{array}{lll}\%C&=&\dfrac{14M_{C}\times 100}{M_{C_{14}H_{22}}}\\\\&=&\dfrac{14\times 12\times 100}{(14\times 12+22\times 1)}\\\\\Rightarrow\%C&=&88.4\end{array}$
$\begin{array}{lll}\%C&=&\dfrac{7M_{C}\times 100}{M_{C_{7}H_{16}}}\\\\&=&\dfrac{7\times 12\times 100}{(7\times 12+1\times 16)}\\\\\Rightarrow\%C&=&84\end{array}$
La bonne réponse est : 5. $C_{7}H_{16}$
Exercice 11
1. Écrivons les formules semi-développées des composés moléculaires.
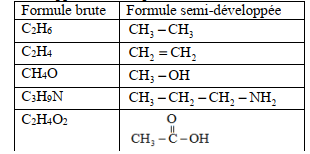
2. Ces données ne suffisent pas pour déterminer la formule A, il faut une donnée supplémentaire la masse molaire par exemple.
Déterminons la formule brute la plus simple
Soit $C_{x}H_{y}O_{z}$ la formule brute du composé
$\begin{array}{rcl} \dfrac{12x}{\%C}&=&\dfrac{y}{\%H}\\&=&\dfrac{16z}{\%O}\\&=&\dfrac{M_{C_{x}H_{y}}O_{z}}{100} \end{array}$
$\begin{array}{rcl} \dfrac{12x}{\%C}&=&\dfrac{y}{\%H}\\ \Rightarrow\,y&=&\dfrac{12x\times\%H}{\%C}\\&=&\dfrac{12x\times6.7}{40}\\ \Rightarrow\,y&=&2x \end{array}$
$\begin{array}{rcl} z&=&\dfrac{12x\times\%O}{\%C\times 16}\\&=&\dfrac{12x\times53}{40\times16}\\ \Rightarrow\,z&=&x \end{array}$
$\begin{array}{rcl} M_{C_{x}H_{y}O_{z}}&=&12x+y+16z\\ \Rightarrow\,M_{C_{x}H_{y}O_{z}}&=&12x+2x+16x\\ \Rightarrow\,M_{C_{x}H_{y}O_{z}}&=&30x \end{array}$
$\begin{array}{rcl} M_{C_{X}H_{y}O_{z}}&=&30\;g\cdot mol^{-1}\\ \Rightarrow\,30x&=&30\\ \Rightarrow\,x&=&1\\ \Rightarrow\,y&=&2\\ \Rightarrow\,z&=&1\\ \Rightarrow\,CH_{2}O \end{array}$
3. Trouvons la formule brute de la saccharine.
Soit $C_{x}H_{y}O_{z}N_{y}S$ la formule brute du composé
$\begin{array}{rcl} \dfrac{12x}{\%C}&=&\dfrac{y}{\%H}\\&=&\dfrac{16z}{\%O}\\&=&\dfrac{14_{t}}{\%N}\\&=&\dfrac{32}{\%S} \end{array}$
$\begin{array}{rcl} \dfrac{12_{x}}{\%C}&=&\dfrac{32}{\%S}\\ \Rightarrow\,x&=&\dfrac{32\times\%C}{12\times\%S}\\&=&\dfrac{32\times45.9}{12\times17.5}\\ \Rightarrow\,x&=&1 7 \end{array}$
$\begin{array}{rcl} y&=&\dfrac{32\times\%H}{1\times\%S}\\&=&\dfrac{32\times2.7}{1\times17.5}\\ \Rightarrow\,y&=&5 \end{array}$
$\begin{array}{rcl} z&=&\dfrac{32\times\%O}{16\times S}\\&=&\dfrac{32\times26.2}{16\times17.5}\\ \Rightarrow\,z&=&3 \end{array}$
$\begin{array}{rcl} t&=&\dfrac{32\times\%N}{14\times\%S}\\&=&\dfrac{32\times7.7}{14\times17.5}\\ \Rightarrow\,t&=&1\\ &\Rightarrow&C_{7}H_{5}O_{3}NS \end{array}$
Exercice 12
1. Les masses moléculaires relatives des composé $X$, $Y$ et $Z$
$M=29d$
$\begin{array}{rcl} M_{x}&=&29\times0.967\\ \Rightarrow\,M_{x}&=&28\;g\cdot mol^{-1} \end{array}$
$\begin{array}{rcl} M_{y}&=&29\times0.893\\ \Rightarrow\,M_{y}&=&26\;g\cdot mol^{-1} \end{array}$
$\begin{array}{rcl} M_{z}&=&29\times1.519\\ \Rightarrow\,M_{z}&=&44\;g\cdot mol^{-1} \end{array}$
2. Les masses d'un litre de chacun des composés gazeux $X$, $Y$ et $Z$
$\begin{array}{rcl} PV&=&nRT\\&=&\dfrac{m}{M}RT\\ \Rightarrow\,m&=&\dfrac{PVM}{RT} \end{array}$
$\begin{array}{rcl} m_{x}&=&\dfrac{PVM_{x}}{RT}\\&=&\dfrac{101325\times1\times28}{8.314\cdot10^{3}\times273}\\ \Rightarrow\,m_{x}&=&1.25\;g \end{array}$
$\begin{array}{rcl} m_{y}&=&\dfrac{PVM_{x}}{RT}\\&=&\dfrac{101325\times1\times26}{8.314\cdot10^{3}\times273}\\ \Rightarrow\,m_{y}&=&m_{y}\\&=&1.16\;g \end{array}$
$\begin{array}{rcl} m_{z}&=&\dfrac{PVM_{x}}{RT}\\&=&\dfrac{101325\times1\times44}{8.314\cdot10^{3}\times273}\\ \Rightarrow\,m_{z}&=&1.96\;g \end{array}$
3. Déterminons les formules moléculaires des trois composés $X$, $Y$ et $Z$
Soit $CxxnOz$ la formule brute du composés $X$
$\begin{array}{rcl} \dfrac{12x}{\%C}&=&\dfrac{y}{\%H}\\&=&\dfrac{M}{100}\\ \Rightarrow\dfrac{12x}{\%C}&=&\dfrac{M}{100}\\ \Rightarrow\,x&=&\dfrac{M\times\%C}{12\times100}\\&=&\dfrac{28\times42.8}{12\times100}\\ \Rightarrow\,x&=&1 \end{array}$
$\begin{array}{rcl} M_{x}&=&12x+16_{z}\\&=&28\\ \Rightarrow\,z&=&\dfrac{28-12\times1}{16}\\ \Rightarrow\,z&=&\\ &\Rightarrow&\,CO \end{array}$
Soit $C_{x}H_{y}$ la formule bruite du composé
$\begin{array}{rcl} \dfrac{12x}{\%C}&=&\dfrac{y}{\%H}\\&=&\dfrac{M}{100}\\ \Rightarrow\dfrac{12x}{\%C}&=&\dfrac{M}{100}\\ \Rightarrow\,x&=&\dfrac{M\times\%C}{12\times100}\\&=&\dfrac{44\times81.8}{12\times100}\\ \Rightarrow\,x &=&3 \end{array}$
$\begin{array}{rcl} M_{x}&=&12x+y\\&=&44\\ \Rightarrow\,y&=&44-3x\\&=&44-3\times12\\ \Rightarrow\,y&=&8\\ \Rightarrow\,C_{2}H_{8} \end{array}$
Exercice 13
1. Établissons la relation qui permet de calculer la masse molaire d'un composé gazeux à partir de sa densité
$\begin{array}{rcl} d&=&\dfrac{m_{\text{Gaz}}}{m_{\text{Air}}}\\&=&\dfrac{\rho_{\text{Gaz}}V}{\rho_{\text{Air}}V} \end{array}$ ;
$\begin{array}{rcl} \text{Pour }V&=&V_{m}\\ \Rightarrow\,d&=&\dfrac{\rho_{\text{Gaz}}V_{m}}{\rho_{\text{Air}}V_{m}} \end{array}$ ;
$\begin{array}{rcl} \text{Or }\rho V_{m}&=&M\\ \Rightarrow\,d&=&\dfrac{M_{\text{Gaz}}}{\rho_{\text{Air}}V_{m}} \end{array}$
2. Calcul de la masse molaire d'un composé gazeux dont la densité est égale à $2.83.$
La masse volumique de l'air est égale à $1.29\;g\cdot L^{-1}$
$\begin{array}{rcl} d&=&\dfrac{M_{\text{Gaz}}} {\rho_{\text{Air}}V_{m}}\\ \Rightarrow\,M_{\text{Gaz}}&=&d\rho_{\text{Air}}V_{m}\\&=&2.83\times1.29\times22.4\\ \Rightarrow\,M_{\text{Gaz}}&=&81.8\;g\cdot mol^{-1} \end{array}$
Exercice 14
1. Calcul de la masse de carbone et de la masse d'hydrogène contenues dans l'échantillon.
$\begin{array}{rcl} n_{c}&=&n_{co_{2}}\\ \Rightarrow\dfrac{m_{c}}{M_{c}}&=&\dfrac{m_{co_{2}}}{M_{co_{2}}}\\ \Rightarrow\,m_{c}&=&\dfrac{m_{co_{2}}}{M_{co_{2}}}\\&=&\dfrac{0.265}{44}\times 12\\ \Rightarrow\,m_{c}&=&0.0723\,g \end{array}$
$\begin{array}{rcl} n_{H}&=&2n_{H_{2}O}\\ \Rightarrow\dfrac{m_{H}}{M_{H}}&=&\dfrac{2m_{H_{2}o}}{M_{H_{2}O}}\\ \Rightarrow\,m_{H}&=&\dfrac{2m_{H_{2}O}}{M_{H_{2}O}}\,M_{H}\\&=&\dfrac{2\times 0.106}{18}\times 1\\\Rightarrow\,m_{H}&=&0.0118\,g \end{array}$
2. Calcul du pourcentage massique de chaque élément.
$\begin{array}{rcl} \%C&=&\dfrac{m_{c}\times 100}{m_{\text{Compsé}}}\\&=&\dfrac{0.0723\times 100}{0.084}\\\Rightarrow\%C&=&86 \end{array}$
$\begin{array}{rcl} \%H&=&\dfrac{m_{H}\times 100}{m_{\text{Compsé}}}\\&=&\dfrac{0.0118\times 100}{0.084}\\\Rightarrow\%H&=&14 \end{array}$
Exercice 15
1. Calculons les masses de carbone, d'hydrogène et d'oxygène contenues dans l'échantillon.
$\begin{array}{rcl} m_{C}&=&\dfrac{m_{CO_{2}}}{M_{CO_{2}}}M_{C}\\&=&\dfrac{0.886}{44}\times12\\\Rightarrow\,m_{C}&=&0.242\,g \end{array}$
$\begin{array}{rcl} m_{H}&=&\dfrac{2m_{H_{2}O}}{M_{H_{2}O}}M_{H}\\&=&\dfrac{2\times0453}{18}\times 1\\\Rightarrow\,m_{H}&=&0.0503\,g \end{array}$
$\begin{array}{rcl} m_{o}&=&m-\left(m_{H}+m_{C}\right)\\&=&0.375-(0.0503+0.242)\\\Rightarrow\,m_{o}&=&0.0827\,g \end{array}$
2. Déterminons la formule brute de $(A)$ sachant que sa masse molaire est égale à $74\,g\cdot mol^{-1}.$
Soit $C_{x}H_{y}O_{z}$ la formule brute du composé.
$\begin{array}{rcl} \dfrac{12X}{\%C}&=&\dfrac{M}{100}\\\Rightarrow\,x&=&\dfrac{M\times\%C}{12\times100} \end{array}$ ;
$\begin{array}{rcl} \text{Or }\%C&=&\dfrac{m_{C}\times100}{m_{\text{Composé}}}\\\Rightarrow\,x&=&\dfrac{M\times m_{C}\times 100}{12\times100_{m_{\text{Compsé}}}}\\&=&\dfrac{M\times m_{C}}{12\times m_{\text{Compsé}}}\\&=&\dfrac{74\times0.242}{12\times 0.375}\\\Rightarrow\,x&=&4 \end{array}$
$\begin{array}{rcl} y&=&\dfrac{M\times m_{H}}{1\times m_{\text{Compsé}}}\\&=&\dfrac{74\times 0.0503}{1\times 0.375}\\\Rightarrow\,y&=&10 \end{array}$
$\begin{array}{rcl} z&=&\dfrac{M\times m_{O}}{16\times m_{\text{Compsé}}}\\&=&\dfrac{74\times 0.0827}{16\times 0.375}\\\Rightarrow\,z&=&1\\&\Rightarrow&\,C_{4}H_{10}O \end{array}$
Exercice 16
Déterminons sa formule brute
Soit $C_{x}H_{y}O_{z}$ la formule brute du composé
Soit $C_{x}H_{y}O_{z}$ la formule brute du composé
$\begin{array}{rcl} x&=&\dfrac{M\times\%C}{12\times100}\\&=&\dfrac{152\times 78.9}{12\times 100}\\\Rightarrow\,x&=&10 \end{array}$
$\begin{array}{rcl} y&=&\dfrac{M\times\%H}{1\times}\\&=&\dfrac{152\times10.5}{1\times100}\\\Rightarrow\,y&=&16 \end{array}$
$\begin{array}{rcl} z&=&\dfrac{M\times\%O}{16\times 100}\\&=&\dfrac{152\times10.5}{16\times 100}\\\Rightarrow\,z&=&1\\&\Rightarrow&\,C_{10}H_{16}O \end{array}$
Exercice 17
Déterminons sa formule brute
Soit $C_{x}H_{y}N_{z}$ la formule brute du composé
$\begin{array}{rcl} x&=&\dfrac{M\times\%C}{12\times 100}\\&=&\dfrac{59\times 40.6}{12\times 100}\\\Rightarrow\,x&=&2 \end{array}$
$\begin{array}{rcl} y&=&\dfrac{M\%H}{1\times100}\\&=&\dfrac{59\times8.47}{1\times 100}\\\Rightarrow\,y&=&5 \end{array}$
$\begin{array}{rcl} z&=&\dfrac{M\times\%N}{14\times 100}\\&=&\dfrac{59\times23.7}{14\times100}\\\Rightarrow\,z&=&1\\&\Rightarrow&\,C_{2}H_{5}N \end{array}$
Exercice 18
1. Détermination de la composition centésimale de ce composé
$\begin{array}{rcl} \%C&=&\dfrac{m_{C}\times 100}{m_{\text{Compsé}}}\\\text{or }m_{C}&=&\dfrac{m_{co_{2}}\times M_{C}}{M_{co_{2}}}\\\Rightarrow\%C&=&\dfrac{m_{co_{2}}\times M_{C}\times 100}{m_{\text{Compsé}}M_{co_{2}}}\\&=&\dfrac{1.76\times 12\times100}{0.74\times 44}\\\Rightarrow\%C&=&64.9 \end{array}$
$\begin{array}{rcl} \%H&=&\dfrac{m_{H_{2}o}\times2M\times100}{m_{\text{compsé}}M_{H_{2}o}}\\&=&\dfrac{0.9\times2\times1\times100}{0.74\times18}\\\Rightarrow\%H1&=&13.5 \end{array}$
$\begin{array}{rcl} \%N&=&100-\left(\%C+\%H\right)\\&=&100-(64.9+13.5)\\\Rightarrow\%N&=&21.6 \end{array}$
2. Calcul de sa masse molaire
$\begin{array}{rcl} nRT&=&PV\\\Rightarrow\dfrac{m}{M}nRT&=&PV\\\Rightarrow\,M&=&\dfrac{mRT}{PV}\\&=&\dfrac{0.111\times8.314\cdot10^{3}\times 294} {102791\times35.6\cdot10^{-3}}\\\Rightarrow\,M&=&74\,g\cdot mol^{-1} \end{array}$
3. Déterminer sa formule moléculaire
Soit $C_{x}H_{y}N_{z}$ la formule brute du composé
$\begin{array}{rcl} x&=&\dfrac{M\times\%C}{12\times 10}\\&=&\dfrac{74\times64.9}{12\times 100}\\\Rightarrow\,x&=&4 \end{array}$
$\begin{array}{rcl} y&=&\dfrac{M\times\%H}{1\times100}\\&=&\dfrac{74\times13.5}{1\times100}\\\Rightarrow\,y&=&10 \end{array}$
$\begin{array}{rcl} z&=&\dfrac{M\times\%N}{14\times100}\\&=&\dfrac{74\times21.6}{14\times100}\\\Rightarrow\,z&=&1\\\Rightarrow\,C_{4}H_{10}N \end{array}$
4. Écrivons les formules moléculaires semi-développées de 5 isomères non cycliques
$CH_{3}$ - $CH_{2}$ - $CH_{2}$ - $CH_{2}$ - $NH_{2}$
$CH_{3}$ - $CH\left(CH_{3}\right)$ - $CH_{2}$ - $NH_{2}$
$CH_{3}$ - $CH_{2}$ - $CH_{2}$ - $NH$ - $NH$ - $CH_{3}$
$CH_{3}$ - $CH\left(CH_{3}\right)$ - $NH$ - $CH_{3}$
$CH_{3}$ - $CH_{2}$ - $NH$ - $CH_{2}$ - $CH_{3}$
$CH_{3}$ - $C\left(CH_{3}\right)_{2}$ - $NH_{2}$
Exercice 19
La formule brute du glucose
Soit $C_{x}H_{y}O_{z}$ la formule brute du composé
$\begin{array}{rcl} x&=&\dfrac{M\times\%C}{12\times 100}\\&=&\dfrac{180\times40.0}{12\times 100}\\\Rightarrow\,x&=&6 \end{array}$
$\begin{array}{rcl} y&=&\dfrac{M\times\%H}{1\times 100}\\&=&\dfrac{180\times6.7}{1\times 100}\\\Rightarrow\,y&=&12 \end{array}$
$\begin{array}{rcl} z&=&\dfrac{M\times\%O}{16\times 100}\\&=&\dfrac{180\times 53.3}{16\times 100}\\\Rightarrow\,z&=&6\\\Rightarrow\,C_{6}H_{12}O_{6} \end{array}$
Exercice 20
1. Équation de la réaction modélisant cette transformation chimique.
$\begin{array}{rcl} C_{x}H_{y}O_{z}+\left(2x+\dfrac{y}{2}-z\right)CuO\longrightarrow\,xCO_{2}+\dfrac{Y}{2}H_{2}O+\left(2x+\dfrac{Y}{2}-z\right)Cu \end{array}$
2. Quantité de matière du composé organique contenait l'échantillon utilisé
$\begin{array}{rcl} n&=&\dfrac{m}{M}\\&=&\dfrac{230\cdot 10^{-3}}{46}\\\Rightarrow\,n&=&5\cdot10^{-3}mol \end{array}$
3. Exprimons en fonction de $x$ la quantité de matière de dioxyde de carbone et en fonction de $y$ la quantité de matière d'eau produite au cours de la transformation chimique.
$\begin{array}{rcl} n&=&\dfrac{n_{co_{2}}}{x}\\\Rightarrow\,n_{co_{2}}&=&xn\\\Rightarrow\,n_{co_{2}}&=&5\cdot 10^{-3}x \end{array}$
$\begin{array}{rcl} N&=&\dfrac{2n_{H_{2}O}}{y}\\\Rightarrow\,n_{H_{2}O}&=&\dfrac{yn}{2}\\&=&\dfrac{5\cdot10^{-3}y}{2}\\\Rightarrow\,n_{H_{2}O}&=&2.5\cdot10^{-3}y \end{array}$
4. Déduisons les valeurs de $x$, $y$ et $z$ ainsi que la formule brute du composé organique étudié.
$\begin{array}{rcl} n_{co_{2}}&=&5\cdot10^{-3}x\\&=&\dfrac{m_{co_{2}}}{M_{co_{2}}}\\\Rightarrow 5\cdot 10^{-3}x&=&\dfrac{440\cdot10^{-3}}{44}\\\Rightarrow\,x&=&\dfrac{10}{5}\\\Rightarrow\,x&=&2 \end{array}$
$\begin{array}{rcl} n_{H_{2}}O&=&2.5\cdot10^{-3}y\\&=&\dfrac{m_{H_{2}O}}{M_{H_{2}O}}\\\Rightarrow 2.5\cdot 10^{-3}y&=&\dfrac{270\cdot10^{-3}}{18}\\\Rightarrow 2.5y&=&15\\\Rightarrow\,y&=&6 \end{array}$
$\begin{array}{rcl} M&=&12_{x}+y+16_{z}\\&=&46\\\Rightarrow\,z&=&\dfrac{46-(12x+y)}{16}\\&=&\dfrac{46-(12\times2+6}{16}\\\Rightarrow\,z&=&1\\\Rightarrow\,C_{2}H_{6}O \end{array}$
5. Déterminons les pourcentages en masse de chaque élément présent dans ce composé.
$\begin{array}{rcl} \%C&=&\dfrac{m_{CO_{2}}\times M_{C}\times 100}{m_{\text{C}}M_{CO_{2}}}\\&=&\dfrac{440\times12.0\times 100}{230\times44}\\\Rightarrow\%C&=&52.2 \end{array}$
$\begin{array}{rcl} \%H&=&\dfrac{m_{H_{2}O}\times 100}{m_{\text{Compsé}M_{H_{2}O}}}\\&=&\dfrac{270\times 2\times 1.0\times100}{230\times 18}\\\Rightarrow\%H&=&13.0 \end{array}$
$\begin{array}{rcl} \%O&=&100-\left(\%C+\%H\right)\\&=&100-(52.2+13.0)\\\Rightarrow\%O&=&34.8 \end{array}$
Exercice 21
1. Déduisons la composition centésimale molaire de l'élément oxygène
$\begin{array}{rcl} \%O&=&100-\left(\%C+\%H+\%N+\%C1\right)\\&=&100-(65.68+6.78+5.89+14.91)\\\Rightarrow\%O&=&6.74 \end{array}$
2. Déterminons la formule brute du chlorhydrate de kétamine
Soit $C_{x}H_{y}O_{z}N_{t}C_{lu}$ la formule brute du composé
$\begin{array}{rcl} x&=&\dfrac{M\times\%C}{12\times 100}\\&=&\dfrac{237.725\times65.68}{12\times100}\\\Rightarrow\,x&=&13 \end{array}$
$\begin{array}{rcl} y&=&\dfrac{M\times\%H}{1\times 100}\\&=&\dfrac{237.725\times6.78}{1\times 100}\\\Rightarrow\,y&=&16 \end{array}$
$\begin{array}{rcl} z&=&\dfrac{M\times%O}{16\times 100}\\&=&\dfrac{237.725\times6.74}{16\times 100}\\\Rightarrow\,z&=&1 \end{array}$
$\begin{array}{rcl} t&=&\dfrac{M\times\%N}{14\times 100}\\&=&\dfrac{237.725\times5.89}{14\times 100}\\\Rightarrow\,t&=&1 \end{array}$
$\begin{array}{rcl} u&=&\dfrac{M\times\%C1}{35.5\times 100}\\&=&\dfrac{237.725\times14.91}{35.5\times 100}\\\Rightarrow\,u&=&1\\\Rightarrow\,C_{13}H_{16}ONC1 \end{array}$
Exercice 22
1. Déterminons la masse molaire de ce composé
$\begin{array}{rcl} M&=&29d\\&=&29\times 1.58\\\Rightarrow\,M&=&46\,g\cdot mol^{-1} \end{array}$
2. Déduisons sa formule brute
Soit $C_{x}H_{y}O_{z}$ la formule brute du composé
$\begin{array}{rcl} x&=&\dfrac{M\times%C}{12\times 100}\\&=&\dfrac{46\times52.17}{12\times100}\\\Rightarrow\,x&=&2 \end{array}$
$\begin{array}{rcl} y&=&\dfrac{M\times\%H}{1\times 100}\\&=&\dfrac{46\times13.04}{1\times100}\\\Rightarrow\,y&=&6 \end{array}$
$\begin{array}{rcl} z&=&\dfrac{M\times\%O}{16\times 100}\\&=&\dfrac{46\times34.79}{16\times 100}\\\Rightarrow\,z&=&1\\\Rightarrow\,C_{2}H_{6}O \end{array}$
Exercice 23
1. Calculons le rapport $\dfrac{y}{x}$
$\begin{array}{rcl} \%H&=&100-\%C\\&=&100-85.7\\\Rightarrow\%H&=&14.3 \end{array}$
$\begin{array}{rcl} \dfrac{12x}{\%C}&=&\dfrac{y}{\%H}\\\Rightarrow\dfrac{y}{x}&=&\dfrac{12\times%H}{\%C}\\&=&\dfrac{12\times14.3}{85.7}\\\Rightarrow\dfrac{y}{x}&=&2 \end{array}$
2. Déduisons la formule brute de cet hydrocarbure
$\begin{array}{rcl} M&=&29d\\&=&29\times1.93\\\Rightarrow\,M&=&56\,g\cdot mol^{-1} \end{array}$
$\begin{array}{rcl} \dfrac{y}{x}&=&2\\\Rightarrow\,y&=&2x\\\text{or }M&=&12x+y\\&=&56\\\Rightarrow12x+2x&=&56\\\Rightarrow 14x&=&56\\ \Rightarrow\,x&=&\dfrac{56}{14}\\\Rightarrow\,x&=&4\\\Rightarrow\,C_{4}H_{8} \end{array}$
3. Écrire toutes les formules semi-développées possibles de cet hydrocarbure.
$CH_{3}$ - $CH_{2}$ - $CH=CH_{2}$
$CH_{3}$ - $CH=CH$ - $CH_{3}$
$CH_{2}=C\left(CH_{3}\right)$ - $CH_{3}$
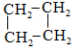
Exercice 24
1. Déterminons la formule brute de cet hydrocarbure.
Équation de la réaction
$\begin{array}{rcl} C_{x}H_{y}+\left(x+\dfrac{y}{4}\right)O_{2}\longrightarrow\,xCO_{2}+\dfrac{y}{2}H_{2}O \end{array}$
D'après le bilan volumique :
$V_{C_{x}H_{y}}=\dfrac{V_{O_{2}}}{x+\dfrac{y}{4}}\\=\dfrac{V_{CO_{2}}}{x}$
$\begin{array}{rcl} V_{C_{x}H_{y}}&=&\dfrac{V_{CO_{2}}}{x}\\\Rightarrow\,x&=&\dfrac{V_{CO_{2}}}{V_{C_{x}H_{y}}}\\&=&\dfrac{30}{10}\\\Rightarrow\,x&=&3 \end{array}$
$\begin{array}{rcl} V_{C_{x}H_{y}}&=&\dfrac{V_{O_{2}}}{x+\dfrac{y}{4}}\\\Rightarrow\,x+\dfrac{y}{4}&=&\dfrac{V_{O_{2}}}{V_{C_{x}H_{y}}}\\&=&\dfrac{50}{10}\\\Rightarrow\,x+\dfrac{y}{4}&=&5\\\Rightarrow\,y&=&4(5-3)\\&=&4(5-3)\\\Rightarrow\,y&=&8\\\Rightarrow\,C_{3}H_{8} \end{array}$
2. Écrivons sa formule semi-développée.
$CH_{3}$ - $CH_{2}$ - $CH_{3}$
Exercice 25
1. Équation chimique de la réaction de combustion.
$C_{x}H_{y}O_{z}+\left(x+\dfrac{y}{4}-\dfrac{z}{2}\right)O_{2}\longrightarrow\,xCO_{2}+\dfrac{y}{2}H_{2}O$
2. Déterminons la formule brute de ce composé.
D'après le bilan molaire :
$\begin{array}{rcl} n_{C_{x}H_{y}}&=&\dfrac{n_{O_{2}}}{x+\dfrac{y}{4}-\dfrac{z}{2}}\\&=&\dfrac{n_{CO_{2}}}{x}\\&=&\dfrac{n_{H_{2}O}}{\dfrac{y}{2}} \end{array}$
$\begin{array}{rcl} n_{C_{x}H_{y}}&=&\dfrac{n_{H_{2}O}}{\dfrac{y}{2}}\\\Rightarrow\,x&=&\dfrac{n_{CO_{2}}}{n_{C_{x}H_{y}}}\\&=&\dfrac{m_{CO_{2}}}{M_{CO_{2}n_{C_{x}H_{y}}}}\\&=&\dfrac{1.32}{44\times0.0}\\\Rightarrow\,x&=&3 \end{array}$
$\begin{array}{rcl} n_{C_{x}H_{y}}&=&\dfrac{n_{H_{2}O}}{\dfrac{y}{2}}\\\Rightarrow\,y&=&\dfrac{2n_{H_{2}O}}{n_{C_{x}H_{y}}}\\&=&\dfrac{2_{m_{H_{2}O}}}{M_{H_{2}O}n_{C_{x}H_{y}}}\\&=&\dfrac{2\times0.72}{18\times0.01}\\\Rightarrow\,y&=&8 \end{array}$
$\begin{array}{rcl} n_{C_{x}H_{y}}&=&\dfrac{n_{O_{2}}}{x+\dfrac{y}{4}-\dfrac{z}{2}}\\\Rightarrow\,x+\dfrac{y}{4}-\dfrac{z}{2}&=&\dfrac{n_{O_{2}}}{V_{m}n_{C_{x}H_{y}}}\\&=&\dfrac{1.08}{24\times0.01}\\&=&4.5\\\Rightarrow\,z&=&2x+\dfrac{y}{2}-9\\\Rightarrow\,z&=&1 \end{array}$
3. Écrivons les formules semi-développées des isomères correspondant à cette formule brute.
$CH_{3}$ - $CH_{2}$ - $CH_{2}OH$
$CH_{3}$ - $CHOH$ - $CH_{3}$
$CH_{3}$ - $CH_{2}$ - $O$ - $CH_{3}$

Commentaires
Souleymane (non vérifié)
dim, 11/26/2023 - 01:51
Permalien
Dabia
Yacine diop (non vérifié)
dim, 11/26/2023 - 22:30
Permalien
Exercices
Yacine diop (non vérifié)
dim, 11/26/2023 - 22:30
Permalien
Exercices
Yacine diop (non vérifié)
dim, 11/26/2023 - 22:30
Permalien
Exercices
Diogo (non vérifié)
sam, 12/21/2024 - 01:33
Permalien
Exercices
Ajouter un commentaire