Série d'exercices sur les Masses : masse volumique et densité - 4e
Classe:
Quatrième
Exercice 1
Compléter le texte ci-dessous par les mots, groupes de mots ou symboles suivants :
gramme, masses marquées, le centigramme, quintal, décakilogramme, masse, le kilogramme , $kg$, décroissant, sous multiple, $t\;,\ 1\,000$, hectogramme, décagramme.
$\centerdot$ La balance permet de déterminer la $\ldots\ldots$ d'un objet.
$\centerdot$ La masse a pour unité internationale $\ldots\ldots$ de symbole $\ldots\ldots$
$\centerdot$ Le décigramme est $\ldots\ldots$ du kilogramme alors que la tonne, de symbole $\ldots\ldots$ en est $\ldots\ldots$ et vaut $\ldots\ldots kg.$
$\centerdot$ Les autres sous multiples sont : $\ldots\ldots$, $\ldots\ldots$
$\centerdot$ Les multiples restant sont : $\ldots\ldots$ et $\ldots\ldots$
$\centerdot$ Avec une balance Roberval, lors de la pesée, on utilise des $\ldots\ldots$ $\ldots\ldots$ pour rééquilibrer la balance.
$\centerdot$ Les masses marquées sont posées dans l'ordre $\ldots\ldots$
Exercice 2
Encadrer la lettre correspondant à la ou les bonnes réponses dans les questions :
1) La masse d'un objet peut s'exprimer en :
a) kilogramme ;
b) mètre cube ;
c) kilogramme par mètre cube ;
d) gramme
2) La tonne est :
a) l'unité du système internationale de masse
b) un multiple du kilogramme
c) un sous multiple du kilogramme
d) égale à mille kilogrammes
3) Pour déterminer la masse d'une voiture, on utilise :
a) une balance Roberval
b) une bascule
c) un pont bascule
4) La masse d'un objet à Dakar est $15\;kg.$
Sa masse au nord de la France sera :
a) plus grande ;
b) plus petite ;
c) la même
Exercice 3
1) En utilisant les puissances de 10, convertir puis donner l'écriture scientifique :
a) $14\;hg=\ldots g$ ;
b) $25\;dag=\ldots kg$ ;
c) $1950\;mg=\ldots g$ ;
d) $2.5\;kg=\ldots g$
e) $150\;g=\ldots mg$ ;
f) $27\;cg=\ldots mg=\ldots hg$
2) On a déterminé la masse d'un objet à l'aide d'une balance Roberval.
Sachant que la masse trouvée est de $m=278\;g$ quelles sont les masses marquées qui sont sur le plateau à la fin de la pesée si la boîte de masses marquées contenait :
$500\;g-200\;g\ 100\;g-100\;g\ 50g-20\;g-10\;g-10\;g-5\;g-2\;g-2\;g-1\;g$
Exercice 4
Compléter le texte ci-dessous par les mots, groupes de mots ou symboles suivants :
le volume, kilogramme par mètre cube, une constante, masse volumique, variable, $kg\cdot m^{-3}$, la masse.
$\centerdot$ La masse de l'unité de volume est appelé $\ldots\ldots$
$\centerdot$ La masse volumique s'exprime en $\ldots\ldots$ de symbole $\ldots\ldots$
$\centerdot$ Pour calculer la masse volumique d'une substance ou d'un corps, on fait le rapport entre $\ldots\ldots$ et $\ldots\ldots$
$\centerdot$ La masse volumique d'un corps pur est $\ldots\ldots$ alors qu'elle est $\ldots\ldots$ pour un mélange.
Exercice 5
Encadrer la lettre correspondant à la (ou les) bonne (s) réponse (s) dans les questions suivantes :
1) La masse volumique $\rho\text{(rho)}$ d'une substance de masse $m$ et de volume $V$ a pour expression :
a) $\rho=\dfrac{m}{V}$ ;
b) $\rho=\dfrac{V}{m}$ ;
c) $r=m\;V$
2) A partir de l'expression de la masse volumique, la masse s'obtient par :
a) $m=\dfrac{\rho}{V}$
b) $m=\dfrac{V}{\rho}$
c) $m=\rho\;V$
3) A partir de l'expression de la masse volumique, le volume s'obtient par :
a) $V=m\rho$
b) $V=\dfrac{m}{\rho}$
c) $V=\dfrac{\rho}{m}$
Exercice 6
1 La masse d'un volume $V=0.5\;L$ d'essence est $0.35\;kg.$
a) Donner l'expression de la masse volumique.
b) Calculer la masse volumique de l'essence en $kg\cdot L^{-1}$ puis en $kg\cdot m^{-3}$ et en $g\cdot L^{-1}.$
2) Calculer le volume en $dm^{3}$ de $58.5\;kg$ de fer si la masse volumique du fer est $7.8\;g\cdot cm^{-3}$
3) Quel est la masse de $350\;cm^{3}$ d'aluminium sachant que la masse volumique de l'aluminium est $2700\;g\cdot dm^{-3}.$
Exercice 7
On veut déterminer la masse volumique de l'essence.
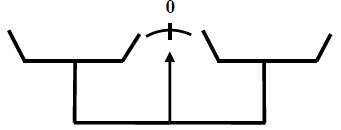
Les opérations de pesage $A\;,\ B\text{ et }C$ ci-dessous ont été réalisées :
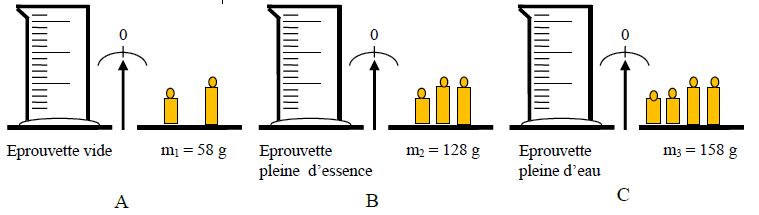
Observer bien les schémas puis répondre à cette série de questions en choisissant la bonne réponse dans chaque cas.
1) Dans l'opération $A$ on a pesé la masse de :
a) Éprouvette ;
b) Essence ;
c) Eau.
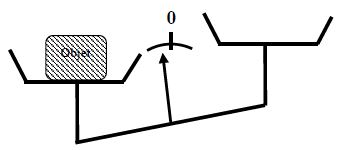
2) Dans l'opération $B$ on a pesé la masse de :
a) Essence
b) Éprouvette plus essence
c) Eau.
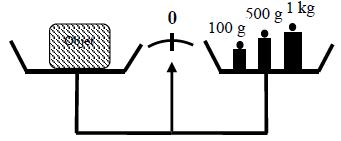
3) Dans l'opération $C$ on a pesé la masse de :
a) Eau ;
b) Éprouvette plus eau ;
c) Éprouvette
La masse de l'essence est :
a) $m_{ess}=m_{3}-m_{1}$
b) $m_{ess}=m_{3}-m_{2}$ ;
c) $m_{ess}=m_{2}-m_{1}$
5) La masse de l'eau est :
a) $m_{eau}=m_{3}-m_{1}$
b) $m_{eau}=m_{3}-m_{2}$
c) $m_{eau}=m_{2}-m_{1}$
6) La masse volumique de l'eau étant de $1\;g\cdot cm^{-3}$ alors le volume de l'eau est :
a) $30\;cm^{3}$
b) $100\;cm^{3}$
c) $70\;cm^{3}$
7) L'essence et l'eau ont :
a) des volumes égaux
b) des volumes différents
8) En s'aidant des réponses données dans les différentes questions, calculer la masse volumique de l'essence.
Exercice 8
Le diamant, pierre précieuse très dure, est du carbone pur.
Sa masse volumique est de $3500\;kg\cdot m^{-3}.$
La densité du diamant par rapport au verre est de 1.4.
Quelle est la masse volumique du verre ?
Exercice 9
La densité du lait est 1.03.
Est-il plus dense que l'eau ? Calculer la masse de 1.5 L de lait.
Exercice 10
Une bouteille de volume 5 L a une masse de 2.7 kg, lorsqu'elle est à moitié remplie d'eau.
Sa masse est de 4.145 kg si elle est remplie d'alcool.
1) Calculer la masse de la bouteille vide sachant que la masse volumique de l'eau est de $1000\;kg\cdot m^{-3}.$
2) Calculer la masse de l'alcool puis en déduire sa masse volumique.
Exercice 11
La densité de l'or par rapport au mercure est de 1.42.
Calculer la masse volumique de l'or en $kg\cdot dm^{-3}$ sachant que celle du mercure est $13.6\;g\cdot mL^{-1}.$
L'or, flotte-t-il dans le mercure ?
Exercice
Pour déterminer la masse volumique d'une boule on a effectué les opérations $A\text{ et }B$ suivantes :
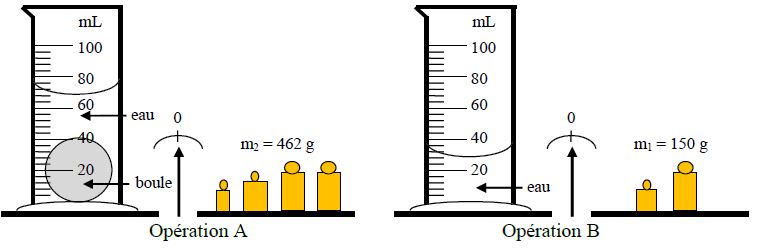
1) A partir du schéma ci-dessus , réduire la masse de la boule ainsi que son volume.
2) Calculer la masse volumique de la boule.
Exercice 12
On veut déterminer la nature d'un métal inconnu $X.$
Pour ce faire, on cherche à déterminer sa masse volumique en réalisant les opérations $A\;,\ B\text{ et }C$ de pesées décrites dans les schémas ci-dessous :
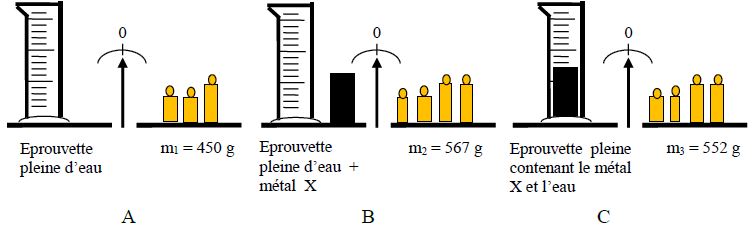
Après avoir bien observé les schémas, déterminer :
1) La masse du métal inconnu $X$
2) La masse de l'eau remplacée par le métal $X$ lorsqu'il est introduit dans le bêcher.
3) Le volume du métal si $\rho_{e}=1\;g\cdot mL^{-1}$
4) Calculer la masse volumique du métal inconnu $X$
5) En utilisant le tableau ci-dessous, donner en justifiant la nature du métal inconnu $X.$
$$\begin{array}{|c|c|c|c|} \hline \text{Métaux}&\text{Aluminium}&\text{Zinc}&\text{Fer}\\ \hline \text{Masse volumique}&2700\;kg\cdot m^{-3}&7100\;kg\cdot m^{-3}&7800\;kg\cdot m^{-3}\\ \hline \end{array}$$
6) Calculer la densité du métal $X$ par rapport à l'huile de masse volumique $920\;g\cdot L^{-1}.$
Exercice 13 Maitrise de connaissances
Recopie et complète les phrases suivantes
La $\ldots\ldots$ d'un corps est une grandeur physique qu'on peut mesurer à l'aide d'une balance.
Elle est exprimée en $\ldots\ldots$ dans le Système International d' Unités
La masse volumique d'un corps solide est la $\ldots\ldots$ de ce corps par unité de $\ldots\ldots$ dans le Système International d'unités, la masse volumique est exprimée en $\ldots\ldots$ par $\ldots\ldots$ que l'on note $\ldots\ldots$
Exercice 14
Réponds par Vrai (V) ou faux (F)
1) Si deux corps ont le même volume, celui qui a la plus grande masse a la plus grande masse volumique.
2) Si deux corps ont la même masse, celui ayant la masse volumique la plus faible occupe le plus petit volume.
3) Deux objets formés de matériaux différents et qui ont la même masse ont des volumes différents.
4) La densité est donnée par le même nombre que la masse volumique exprimée en $g\cdot L^{-1}.$
Exercice 15 Le bon choix
Choisis la réponse correcte.
La masse d'un objet est mesurée avec :
$\centerdot$ une éprouvette graduée
$\centerdot$ une balance,
$\centerdot$ un masse-mètre.
$\centerdot$ un dynamomètre
Exercice 16 Types de balance
Donne le nom de chacune des balances.
Indique un domaine d'activités où est utilisée chacune d'elle.

Exercice 17 Conversion d'unités
Convertis
$12.5\;t=\ldots kg$
$3.9\;g=\ldots kg$
$97.8\;kg\cdot L^{-1}=\ldots g\cdot cm^{-3}$
$0.25\;kg\cdot m^{-3}=\ldots kg\cdot L^{-1}$
$3.86\;kg\cdot m^{-3}=\ldots g\cdot cm^{-3}$
Exercice 18 Ordres de grandeurs de masses
Relie, à l'aide d'une flèche, chaque corps à l'ordre de grandeurs masse.
$$\begin{array}{|ll|} \hline \text{Cheveu}&1.3\;g\\ \hline \text{Mouche}&3\;t\\ \hline \text{La Terre}&75\;kg\\ \hline 1\;l\text{ d'air}&0.1\;mg\\ \hline 1\;l\text{ d'eau}&6\cdot 10^{24}kg\\ \hline \text{Homme adulte}&20\;mg\\ \hline \text{Eléphant}&1\;kg\\ \hline \text{Le soleil}&1.989\cdot 10^{30}kg\\ \hline \end{array}$$
Exercice 19 Calcul de masse volumique
1) Le volume occupé par $0.46\;kg$ d'huile est $0.5\;L.$
Calculer la masse volumique de l'huile en $kg\cdot L^{-1}$ en $kg\cdot m^{-3}\text{ et en }g\cdot L^{-1}$
2) Calcule en $dm^{3}$ le volume d'une masse $m=96.5\;kg$ d'or si la masse volumique de l'or est $19.3\;g\cdot cm^{-3}$
3) Quelle est la masse de $350\;cm^{3}$ d'aluminium si sa masse volumique est $2700\;g\cdot dm^{-3}$
Exercice 20
Des mesures de masses et de volumes effectuées sur plusieurs corps ont conduit au tableau de mesure suivant.
$$\begin{array}{|c|c|c|c|c|c|c|} \hline \text{Corps}&A&B&C&D&E&F\\ \hline m(g)&22.4&46.2&66.8&90.4&114.9&133.0\\ \hline V\left( cm^{3}\right)&2.0&4.1&5.9&8.0&14.7&17.0\\ \hline \end{array}$$
Quels sont les corps constitués de la même substance ?
Exercice 21
Pour déterminer la masse d'un solide S on réalise les expériences suivantes à l'aide d'une balance Roberval
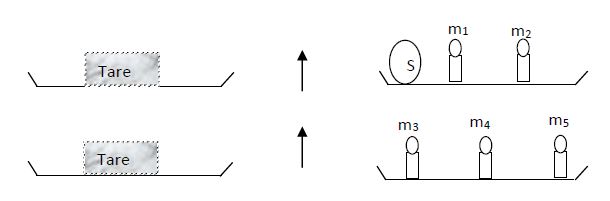
On donne :
$m_{1}=100\;g$ ;
$m_{2}=20\;g$ ;
$m_{3}=200\;g$ ;
$m_{4}=10\;g$ ;
$m_{5}=2\;g$
1) Quel type de pesée a-t-on ainsi réalisé ?
2) Détermine la masse du solide.
3) On plonge ce solide dans une éprouvette contenant un volume $V_{1}=55\;cm^{3}$ d'eau ; le niveau de l'eau remonte jusqu'à $215\;cm^{3}.$ Détermine le volume du solide.
4) Calcule la masse volumique du solide.
En déduire sa densité par rapport à l'eau
Exercice 22
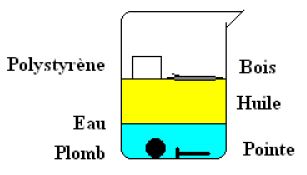
On mélange dans un bécher de l'huile, du mercure et de l'eau.
Indique en justifiant l'ordre dans quel les substances se superposent dans le bécher, du haut vers le bas
Données :
$$\begin{array}{|c|c|c|c|} \hline \text{corps}&\text{huile}&\text{mercure}&\text{eau}\\ \hline \text{Masse volumique}\left(\text{en }g\cdot cm^{-3}\right)&0.87&13.6&1\\ \hline \end{array}$$
Exercice 23
Une bouteille de contenance $5.0\;L$ pèse $2.7\;kg$ lorsqu'elle est à moitié remplie d'eau alors que sa masse est $4.145\;Kg$ si elle est remplie d'alcool.
1) Calculer la masse de la bouteille sachant que la masse volumique de l'eau est $1000\;kg\cdot m^{-3}$
2) Calculer la masse de l'alcool puis en déduire la masse volumique de l'alcool.
Exercice 24
Un bijou constitué d'un alliage d'or et de cuivre de masse $150\;g$ porte l'indication 18 carats.
1) Calculer la masse de l'or et la masse de cuivre contenue dans ce bijou.
2) Calculer le volume de l'or et celui du cuivre dans ce bijou.
3) Calculer la masse volumique de l'alliage
Données :
masse volumique de l'or : $19.3\;g\cdot cm^{-3}$, masse volumique cuivre : $8.9\;g\cdot cm^{-3}$
Un carat correspond à la masse, en gramme d'or pur, dans $24\;g$ d'alliage.
Exercice supplémentaire
1. Ta sœur veut savoir si son collier est fait en or pur.
Aide-la à répondre à sa préoccupation en utilisant les acquis de ton cours.
2. Le bateau « Aline Sitoé Diatta » flotte sur l'eau malgré toutes les charges qu'il supporte alors qu'un petit clou coule rapidement.
En utilisant les acquis du cours de physique, tente de proposer une explication à ces phénomènes observés.
$\begin{array}{c}\blacktriangleright\,\boxed{\text{Correction des exercices}}\end{array}$
Source:
irempt.ucad.sn & ADEM