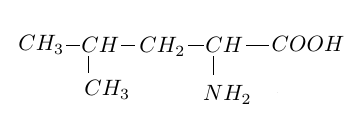Solution des exercices : Les acides carboxyliques - Ts
Classe:
Terminale
Exercice 1
Partie A :
1) Calcul de masse molaire de $(A)$
$\begin{array}{lcl}\dfrac{M_{A}}{100}&=&\dfrac{2M_{0}}{\%O}\\ &\Rightarrow&M_{A}=\dfrac{2M_{0}\times 100}{\%O}\\ &=&\dfrac{2\times 16 \times 100}{31.37}\\ &\Rightarrow&M_{A}=102\,g\cdot mol^{-1} \end{array}$
Détermination de la forme brute de $(A)$
$\begin{array}{lcl} M_{A}&=&M_{C_{n}H_{2n}O_{2}}\\&=&14n+32\\&=&102&\Rightarrow&n=5, \end{array}$
d'où la formule brute : $C_{4}H_{9}COOH$
2) Formules semi-développées possibles :
$CH_{3}-(CH_{2})_{3}-COOH$ : acide pentanoique
$CH_{3}-CH_{2}-CH(CH_{3})-COOH$ : acide$-2-$méthylbutanoique
$CH_{3}-CH_{2}(CH_{3})-CH_{2}-COOH$ : acide$-3-$méthylbutanoique
$(CH_{3})_{3}C-COOH$ : acide$-2.2-$diméthylpropanoique
3) a) Détermination de la concentration de la solution
$\begin{array}{lcl} C_{A}&=&\dfrac{m}{M_{A}V}\\&=&\dfrac{4}{102\times 200\cdot 10^{-3}}\\&\Rightarrow&C_{A}=0.20\,mol\cdot L^{-1} \end{array}$
b) Équation de la réaction
$2C_{5}H_{9}-COOH+Fe\ \rightarrow\ (C_{5}H_{9}COO)_{2}Fe+H_{2}$
Le réactif en excès
$\begin{array}{lcl} \dfrac{n_{A}}{2}&=&\dfrac{m_{A}}{2M_{A}}\\&=&\dfrac{4}{2\times 102\cdot}\\&=&0.020\,mol\ ;\ \\\dfrac{n_{Fe}}{1}&=&\dfrac{2.8}{56}\\&=&0.048\,mol \end{array}$
$\dfrac{n_{Fe}}{1}>\dfrac{m_{A}}{2M_{A}}$ ; le Fer est réactif en excès
Le volume de gaz dégagé
$\begin{array}{lcl} \dfrac{n_{A}}{2}&=&n_{H_{2}}\\&\Rightarrow&V_{H_{2}}=n_{H_{2}}\times V_{m}\\&=&0.02\times 24\\&\Rightarrow&V_{H_{2}}=0.48\,L \end{array}$
Partie B :
1) a) La réaction est appelée réaction d'estérification directe.
b) Elle est lente, limitée et athermique
2) Formule semi-développées et nom de chaque isomère
a) $CH_{3}-CH_{2}-COO-CH_{3}$ : propanoate de méthyle
b) $CH_{3}-COO-CH_{2}-CH_{3}$ : éthanoate d'éthyle
c) $HCOO-CH_{2}-CH_{2}-CH_{3}$ : méthanoate de propyle
d) $HCOO-CH(CH_{3})_{2}$ : méthanoate d'ispropyle ou de $1-$méthyléthyle
3) Formule semi-développée, noms de l'acide et de l'alcool correspondant à chaque isomère de l'ester
a) $CH_{3}-CH_{2}-COOH$ : acide propanoique ; $CH_{3}OH$ : méthanol
b) $CH_{3}-COOH$ : acide éthanoique ; $CH_{3}-CH_{2}OH$ : éthanol
c) $HCOOH$ : acide méthanoique ; $CH_{3}-CH_{2}-CH_{2}OH$ : propan$-1-$ol
d) $HCOOH$ : acide méthanoique ; $CH_{3}-CHOH-CH_{3}$ : propan$-2-$ol
Exercice 2
1) Lors d'une combustion complète d'un composé organique, l'élément carbone est mis en évidence par sa transformation en dioxyde de carbone et l'élément hydrogène en eau
2) Vérification des pourcentages en carbone, en hydrogène dans le composé $C_{n}H_{2n}O_{2}$
Par définition :
$\begin{array}{lcl} \dfrac{12n}{\%C}&=&\dfrac{2n}{\%H}\\&=&\dfrac{32}{\%O}\\&=&\dfrac{M}{100}\\ &\Rightarrow& \dfrac{12n}{\%C}=\dfrac{M}{100}\\&\Rightarrow&\%C=\dfrac{12n\times 100}{M} \end{array}$
Un raisonnement analogue conduit à $H=\dfrac{2n\times 100}{M}\text{ et }\%O=\dfrac{32\times 100}{M}$
b) Montrons que le rapport : $\dfrac{\%C}{\%H}=6$
$\begin{array}{lcl} \dfrac{\%C}{\%H}&=&\dfrac{\dfrac{12n\times 100}{M}}{\dfrac{2n\times 100}{M}}\\ &=&\dfrac{12n\times 100}{M}\times\dfrac{M}{2n\times 100}\\&=&\dfrac{12n}{2n}\\&=&6 \end{array}$
Pourcentages en hydrogène et en oxygène
$\begin{array}{lcl} \dfrac{\%C}{\%H}&=&6\\&\Rightarrow&\%H=\dfrac{\%C}{6}\\&=&\dfrac{54.54}{6}\\&\Rightarrow&\%H=9.09\% \end{array}$
$\begin{array}{lcl} \%O&=&100\%-(\%C+\%H)\\&=&100\%-(54.54\%+9.09\%)\%O\\&=&36.37\% \end{array}$
c) Masse molaire $M$ du composé
$\begin{array}{lcl} \dfrac{M}{100}=\dfrac{32}{\%O}\\&\Rightarrow&M=\dfrac{32\times 100}{36.37}\\&\Rightarrow& M=88\,g\cdot mol^{-1} \end{array}$
Formule brute du composé
$\begin{array}{lcl} M=M_{C_{n}H_{2n}O_{2}}&=&14n+32\\&=&88\\&\Rightarrow&n=4 \end{array}$
d'où la formule brute : $C_{4}H_{8}O_{2}$
3) a) Équation de la réaction
$C_{4}H_{8}O_{2}\ +\ 5O_{2}\ \rightarrow\ 4CO_{2}\ +\ 4H_{2}O$
b) Volume de dioxyde carbone dégagé
D'après le bilan volumique :
$\begin{array}{lcl} \dfrac{V_{A}}{1}=\dfrac{V_{CO_{2}}}{4}\\&\Rightarrow&V_{CO_{2}}=4V_{A}\\&=&4\times 240\,V_{CO_{2}}\\&=&960\,mL \end{array}$
Exercice 3
Nature de la réaction chimique
$C_{n}H_{2n}\ +\ H_{2}O\ \rightarrow\ C_{n}H_{2n+2}O$
Il s'agit d'une réaction d'hydratation
Fonction chimique du produit obtenu
Le produit obtenu par hydratation de l'alcène est un alcool
$M_{C_{n}H_{2n+2}O}=14n+18=88$
$\Rightarrow n=5$
d'où la formule brute : $C_{5}H_{11}OH$
1) Équation de la réaction qui se produit
$CH_{3}-CH_{2}-CH(CH_{3})-COOH+CH_{3}-CHOH-CH_{2}-CH_{2}-CH_{3}\rightleftarrows\\ CH_{3}-CH_{2}-CH(CH_{3})-COOCH(CH_{3})-CH_{2}-CH_{2}-CH_{3}+H_{2}O$
2) Formule semi-développée de ce composé de $A$ et son nom.
L'alcool est secondaire ; son oxydation ménagée conduit à une cétone de formule semi-développée :
$CH_{3}-CO-CH_{2}-CH_{2}-CH_{3}$ : pentan$-2-$one
Exercice 4
1) Groupe fonctionnel caractéristique et nom des composés
$$\begin{array}{|c|c|c|} \hline \text{Composé et groupe fonctionnel}&\text{Nom du groupe fonctionnel}&\text{Nom du composé}\\ \hline A\ :\ CH_{3}-CH_{2}-CH_{2}-\boxed{OH}&\text{Hydroxyle}&\text{Propan}-1-\text{ol}\\ \hline B\ :\ CH_{3}-CH\boxed{OH}-CH_{3}&\text{Hydroxyle}&\text{Propan}-2-\text{ol}\\ \hline C\ :\ CH_{3}-CH_{2}-\boxed{COCl}&\text{Chlorure d'acide}&\text{Chlorure de propanoyle}\\ \hline D\ :\ CH_{3}-CH_{2}-\boxed{COO}CH_{2}-CH_{3}&\text{Ester}&\text{Propanoate d'éthyle}\\ \hline E\ :\ CH_{3}-\boxed{CO-NH_{2}}&\text{Amide}&\text{Etanamide}\\ \hline \end{array}$$
2) a) Équation-bilan des réactions
Demi-équations électroniques :
$3\left(CH_{3}-CH_{2}-CH_{2}-OH\ \rightarrow\ CH_{3}-CH_{2}-CHO+2H^{+}+2e\right)$
$CrO_{7}^{2-}+14H^{+}+6e\ \rightarrow\ 2Cr^{3+}+7H_{2}O$
Équation-bilan de la première étape :
$3CH_{3}-CH_{2}-CH_{2}-OH+Cr_{2}O_{7}^{2-}+8H^{+}\ \rightarrow\ 3CH_{3}-CH_{2}-CHO+2Cr^{3+}+7H_{2}O$
Demi-équation électroniques :
$3\left(CH_{3}-CH_{2}-CH_{2}+H_{2}O\ \rightarrow\ CH_{3}-CH_{2}-COOH+2H^{+}+2e\right)$
$CrO_{2}O_{7}^{2-}+14H^{+}+6e\ \rightarrow\ 2Cr^{3+}+7H_{2}O$
Équation--bilan de la deuxième étape
$3CH_{3}-CH_{2}-CH_{2}-OH+Cr_{2}O_{7}^{2-}+8H^{+}\ \rightarrow\ 3CH_{3}-CH_{2}-COOH+2Cr^{3+}+4H_{2}O$
b) Formule semi développée $H$
L'oxydation ménagée de $B$, alcool secondaire, donne la cétone $H$ de formule semi-développée :
$CH_{3}-CO-CH_{3}$
c) Nature $F$, $G$, et $H$ sont respectivement un aldéhyde, un acide carboxylique et cétone le réactif de Schiff permet de distinguer $F$ et $H$
$F\ :\ CH_{3}-CH_{2}-CHO$ : propanal
$G\ :\ CH_{3}-CH_{2}-COOH$ : acide propanoique
$H\ :\ CH_{3}-CO-CH_{3}$ : propanone
3) Réactions successives possibles permettant d'obtenir $C$ à partir de $A$
$CH_{3}CH_{2}-CH_{2}-OH+\dfrac{1}{2}O_{2}\ \rightarrow\ CH_{3}-CH_{2}-CHO+H_{2}O$
$CH_{3}-CH_{2}-CHO+\dfrac{1}{2}O_{2}\ \rightarrow\ CH_{3}-CH_{2}-COOH$
$CH_{3}-CH_{2}-COOHPCl_{5}\ \rightarrow\ CH_{3}-CH_{2}-COCl+POCl_{3}+HCl$
4) a) Formules semi-développée et noms pour $I$
$\begin{array}{lcl} M_{C_{n}H_{2n}O_{2}}&=&29d\\&\Rightarrow&14n+32=29\times3\\&\Rightarrow&n=4 \end{array}$
d'où la formule brute $\boxed{C_{4}H_{8}O_{2}}$
$CH_{3}-CH_{2}-CH_{2}-COOH$ : acide butanoique
b) Équation-bilan de la réaction
$CH_{3}-CH_{2}-CH_{2}-COOH+CH_{3}-CHOH_{3}\rightleftarrows CH_{3}-CH_{2}-CH_{2}-COO-CH_{2}-CH\left(CH_{3}\right)-CH_{3}+H_{2}O$
$J\ :\ CH_{3}-CH_{2}-CH_{2}-COO-CH_{2}-CH\left(CH_{3}\right)-CH_{3}$ : butanoate d'isobutyle
$-\ \ $Caractéristiques de la réaction :
La réaction est lente, limitée et athermique
Formule semi-développée et le nom d'un composé $K$
$CH_{3}-CH_{2}-COCl$ : chlorure de butanoate
Exercice 5
1) Un triglycéride est triester (ou ester) du glycérol
2) Formule semi-développée de la molécule du glycérol
$CH_{2}OH-CHOH-CH_{2}Oh$
3) L'acide palmitique est u acide gras saturé car sa formule vérifie $C_{n}H_{2n+1}-COOH$ avec $n=15.$
4) Il faut molécule d'eau pour hydrolyser un ester ; donc trois molécules d'eau pour un triester
5) Équation de l'hydrolyse de la palmitine
$C_{15}H_{31}-CO-O-CH_{2}$
$C_{15}H_{31}-CO-O-CH+3H_{2}O\rightleftarrows 3C_{15}H_{31}COOH+CH_{2}OH-CHOH-CH_{2}OH$
$C_{15}H_{31}-CO-O-CH_{2}$
6) Cet état final se nomme état d'équilibre.
Son origine est due à la réaction d'estérification ; réaction inverse de la réaction d'hydrolyse.
Exercice 6
1) a) Un alcool a pour formule générale :
$C_{n}H_{2n+1}OH$
b) L'alcool, subit une oxydation ménagée par le désoxygène de l'air pour donner un composé intermédiaire qui, avec le dioxygène en excès, se transforme $(B)$ qui rougit le $pH$ le désoxygène en excès.
c) le composé $(B)$ est un acide carboxylase de formule générale :
$C_{n}H_{2n+1}COOH$
2) a) Quantité de matière de $(B)$
A l'équivalence :
$\begin{array}{lcl} n_{B}&=&n_{NaOH}\\&\Rightarrow&n_{B}=C_{b}V_{b}\\&=&1\times 27\cdot 10^{-3}\\&=&27\cdot 10^{-3}mol \end{array}$
Nombre de môles de $(A)$ :
$n_{B}=n_{A}=27\cdot 10^{-3}mol$
b) Calcule la masse molaire de $(A).$
$\begin{array}{lcl} M_{A}&=&\dfrac{m}{n_{A}}\\&=&\dfrac{2}{27\cdot 10^{-3}}\\&\Rightarrow&\boxed{M_{A}=74\,g\cdot mol^{-1}} \end{array}$
Noms et sa formule semi-développé de $(A)$
$\begin{array}{lcl} M_{A}&=&M_{C_{n}H_{2n+2}O}\\&=&14n+18\\&=&74\\&\Rightarrow&n=4 \end{array}$
d'où la formule brute : $\boxed{C_{4}H_{9}OH}$
$(A)$, alcool à chaine linéaire, donne par oxydation ménagée dans un excès de dioxygène un acide carboxylique ; $(A)$ est donc alcool primaire de semi-développée :
$CH_{3}-CH_{2}-CH_{2}-CH_{2}OH$ : butan$-1-$ol
c) Formule semi-développée du composé $(B)$ et son nom
$CH_{3}-CH_{2}-CH_{2}-COOH$ : acide butanoique
3) Formule semi-développée du composé $(C)$ formé serait un aldéhyde de formule semi-développée :
$CH_{3}-CH_{2}-CH_{2}-CHO$ : butanal
4) a) Il s'agit d'une déshydratation intermoléculaire
b) Équation de la réaction :
$2CH_{3}-CH_{2}-CH_{2}-CH_{2}OH\stackrel{Al_{2}O_{3}}{\longrightarrow}_{350^{\circ}}CH_{3}-CH_{2}-CH_{2}-CH_{2}-O-CH_{2}-CH_{2}-CH_{2}-CH_{3}$
Le produit formé est $1-$ butoxybutane appartenant à la famille des éthers-oxydes
Exercice 7
1) Montrons que le mélange initial est équimolaire
$-\ $ Nombre de môles de l'acide :
$\begin{array}{lcl} n_{ac}&=&\dfrac{m_{ac}}{M_{ac}}\\&=&\dfrac{12}{(12\times 2+4\times 1+16\times 2)}\\&\Rightarrow&n_{ac}=0.2\,mol \end{array}$
$-\ $ Nombre de môles de l'alcool :
$\begin{array}{lcl} n_{al}&=&\dfrac{m_{al}}{M_{al}}\\&=&\dfrac{12}{(12\times 3+8\times 1+16)}\\&\Rightarrow&n_{al}=0.2\,mol \end{array}$
$n_{ac}=n_{al}$ : le mélange est bien éqimolaire
Calcul de la composition initiale dans le tube :
$-\ $ Nombre de môles de l'acide dans un tube :
$\begin{array}{lcl} n_{ac}&=&\dfrac{n_{ac}}{10}\\&=&\dfrac{0.2}{(10}\\&\Rightarrow&n_{ac}=0.02\,mol \end{array}$
Chaque tube contient initialement $0.02\,mol$ de l'acide éthanoique et $0.02\,mol$ de l'alcool.
2) Équation de la réaction :
$CH_{3}-COOH+CH_{3}-CH_{2}-CH_{2}OH\leftrightarrows CH_{3}COO-CH_{2}-CH_{2}-CH_{3}+H_{2}O$
3) a La température accélère la réaction.
L'acide sulfurique joue le rôle de catalyseur qui accélère aussi la réaction.
b) Le virage de l'indicateur coloré permet de connaitre expérimentalement le point d'équivalence.
c) La date $t=160\,min$ représente l'état d'équilibre au système chimique
$-\ $ Nombre de môles d'ester formé :
$\begin{array}{lcl} n_{ester}&=&\left(n_{ac}\right)_{0}-n_{acide\;restant}\\&=&20\cdot 10^{-3}-6.66\cdot 10^{-3}\\&\Rightarrow&n_{ester}=13.34\cdot 10^{-3}\,mol \end{array}$
d) Calcul le volume de soude $V_{éq}$ versé au cours du dosage à la date $t=160\,min$
On a :
$\begin{array}{lcl} n_{acide\;restant}&=&n_{NaOH_{0}}-n_{acide\;restant}\\&=&20\cdot 10^{-3}-6.66\cdot 10^{-3}\\&\Rightarrow&n_{ester}=13.34\cdot 10^{-3}\,mol \end{array}$
Comparons les volumes $V_{1}$ et $V_{2}$ de soude versés respectivement aux dates $t_{1}=100\,min$ et $t_{2}=200\,min$ au volume $V_{eq}$
$\begin{array}{lcl} V_{1}&=&\dfrac{n_{acide\;restant}}{C_{b}}\\&=&\dfrac{6.8\cdot 10^{-3}}{1}\\&\Rightarrow& \boxed{V_{1}=6.8\,mL} \end{array}$
$\begin{array}{lcl} V_{2}&=&\dfrac{n_{acide\;restant}}{C_{b}}\\&=&\dfrac{6.66\cdot 10^{-3}}{1}\\&\Rightarrow& \boxed{V_{2}=6.7\,mL} \end{array}$
Conclusion :
$V_{éq}\simeq V_{1}\ ;\ V_{éq}\simeq V_{2}$