Série d'exercices : Interférences lumineuses - Ts
Exercice 1
Exercice 2
Exercice 3
Exercice 4
Exercice 5
Exercice 6
Exercice 7
AN :
A.N :
Exercice 8
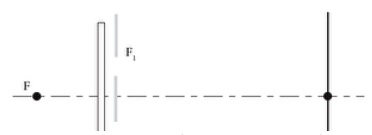
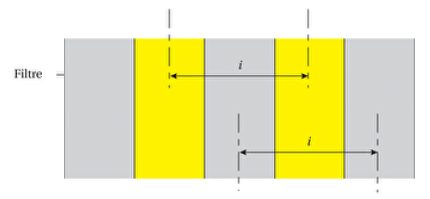
Exercice 9
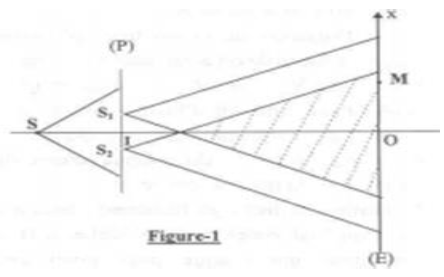
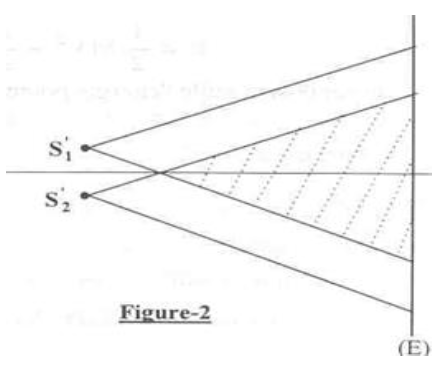
Exercice 10






Notre planète est entourée d'une couche d'air dont la plus grande partie est répartie sur une épaisseur d’une dizaine de kilomètres. On appelle pression atmosphérique la pression qu'exerce cette couche d'air sur les corps à la surface de la Terre. Le symbole de la pression est $P$. La pression atmosphérique est une donnée précieuse pour la météorologie car les mouvements des masses d'air en altitude sont responsables de l'évolution du climat. La mesure de la pression atmosphérique est donc nécessaire pour prévoir les conditions climatiques. L'unité légale de la pression est le pascal (symbole : $Pa$). La pression atmosphérique est mesurée par un appareil de mesure : le baromètre. Certains baromètres sont gradués en hectopascals (symbole : $hPa$) ou en millibars (symbole : mbar). D'autres baromètres sont gradués en hauteur de colonne de mercure (symbole : $mm Hg$).
1.1. Quel instrument de mesure est cité dans ce texte ?
1.2. Que mesure cet instrument ?
1.3. Quel est le symbole de la pression ?
1.4. Quelle est l'unité de pression dans le système international ? Quel est son symbole ?
1.5. Donner les autres unités de pression citées dans le texte. Donner le symbole de chacune, de ces unités.
1.6. Convertir un hectopascal en pascal.
1.7. A part les laboratoires de météorologie, dans quels lieux trouve – t – on des appareils qui permettent de mesurer la pression ? Qui les utilisent ?
On considère les mesures suivantes :
| $A = 26000 x 10^{ 5} m$ | $B = 450 x 10^{– 7} m$ | $C = 606 x 10 m$ |
| $D = 0,0108 x 10^{ – 4} m$ | $E = 0,019 x 10 ^{4} m$ | $ F = 0,0170x 10^{– 7} m$ |
1)- Ecrire ces mesures en utilisant la notation scientifique tout en conservant la précision.
2)- Indiquer le nombre de chiffres significatifs pour chaque mesure.
3)- Donner un ordre de grandeur pour chaque mesure.
4)- Placer ces ordres de grandeurs sur une échelle adaptée. Que peut-on dire de cette échelle ? Justifier.
Fais correspondre par une flèche chaque expression à la bonne réponse.
Recopie et complète les phrases ci-dessous avec les expressions suivantes :filtration, mélange
homogène, mélange hétérogène, décantation, distillation, de l’eau.
2.1. Dans un jus d’orange, il y a de la pulpe d’orange, du sucre, et … La pulpe se dépose : le jus
d’orange constitue un ………… Le jus filtré est un …………
2.2 La boue se dépose au fond d’un lac par ………… L’eau qui pénètre dans le sol, traverse les
couches de sable par ………… et devient limpide.
2.3 Lors d’une pénurie d’eau, une ménagère puise de l’eau dans un puits.
Cette eau est un mélange ………… Elle la laisse au repos dans un récipient pendant quelques
minutes. Des particules lourdes se déposent au fond du récipient par … Elle transvase l’eau dans une
bassine à travers un morceau de gaze pour retenir les particules légères : cette opération appelée
…; elle donne un mélange …………
1. Recopie et complète le tableau ci-dessous
| Grandeursphysiques | Unités | Symboles de l’unité | Instrument de mesure |
| Mètre cube | |||
| Masse | |||
| règle | |||
| Température | |||
| seconde |
2.Une longueur est mesurée avec une règle graduée en cm.
5.1 Choisis l’écriture correcte de la valeur mesurée.
a. $13,00 cm$
b. $13,0 cm$
c. $13,000cm$
d. $13cm$
5.2 Donne une explication au rejet de chacune des autres valeurs.
Pour introduire la leçon sur les grandeurs physiques, un professeur demande aux élèves comparer deux
de leurs camarades par leurs traits physiques.
Associe à chaque trait physique une grandeur physique, si possible
a. Doudou est plus grand que Dominique.
b. Dominique est plus beau que doudou.
c. Dominique est moins gros que Doudou.
d. Doudou est plus âgé que Dominique.
e. Doudou est plus rapide que Dominique.
Prénom……… Nom……………
Fais correspondre par une flèche chaque expression à la bonne réponse.
Lire attentivement ce texte avant de répondre aux questions
La chimie organique apparaît d'abord dans l'histoire comme lachimie des composés du carbone et concerne les substancesdont l'origine est un être vivant, animal ou plante.
Les scientifiques pensaient, au début du $XIXème$ siècle, queles corps “ organiques ” ne pouvaient être produits que par les“ organismes ” végétaux ou animaux. Ceux-ci en effet auraientpossédé une force spéciale, propre à la vie. Le chimiste n'étaitpas en mesure d'insuffler, au cours d'une synthèse, aux
éléments inanimés la force vitale qui leur faisait défaut. Cettepensée vitaliste est à l'origine du retard que le chimiste avaitpris dans la synthèse des corps organiques.
Il faut attendre1828 pour que soit réalisée la premièresynthèse d'une molécule dite organique : le chimiste allemandF. Wöhler obtient alors de l'urée, identifiable à un échantillonauthentique naturel, par décomposition thermique d'uncomposé minéral, le cyanate d'ammonium. “ Je peux faire del'urée sans avoir besoin de reins ou même d'un animal, fût-il homme ou chien ”, écrit Wöhler.
L'essor de la synthèse de molécules organiques prend alors son élan. La complexité desstructures a obligé très rapidement les chimistes à étudier les liaisons entre les atomesconstituants les molécules et à les représenter par des écritures conventionnelles bien établies
maintenant.
Rédigé à partir de $B$. Vidal, Histoire de la chimie, $© PUF$
Coll. “ Que sais-je ? ”, $n°35$,.$2 ème$ éd., $1998$.
Questions :
1.1. Donner un titre à ce texte
1.2. Quelle est l’origine de la chimie organique ? Pourquoi l’a-t-on qualifié « d’organique » ?
1.3.Qu’est-ce qui explique le développement très tardif de la chimie organique ?
1.4. Expliquer en quoi la découverte de Wöhler, a révolutionné la chimie organique et permis
son essor ?
1.5. Une « autre » chimie était beaucoup plus développée à l’époque. Aujourd’hui on luidonne le nom de « chimie inorganique ». Quel autre nom plus courant lui donne-t-onaussi ?
1.6. Justifier alors la phrase du texte « La chimie organique apparaît d'abord dans l'histoire commela chimie des composés du carbone ».
2.1.Compléter les phrases suivantes avec le mot ou le groupe de mots qui conviennent
Les hydrocarbures saturés acycliques ont pour formule …. et sont appelés alcanes.
Les hydrocarbures saturés cycliques sont appelés …. Les monocycliques ont pour formule $C_{n}H_{2}n$
Pour nommer un alcane ramifié, on commence par repérer la …. C'est la chaîne linéaire renfermant le nombre maximum d'atomes de carbone
2.2. Le cétane $C_{16}H_{34}$ est le constituant essentiel du gazole. Sa combustion complète dans l’oxygène de l’air donne du dioxyde de carbone et de l’eau.
Recopier et équilibrer l’équation de la combustion suivante
$C_{16}H_{34} + …… O_{2}\rightarrow{…… CO_{2} } + …… H_{2} O$
2.3. Indiquer, en recopiant leur formule brute sur la copie, les alcanes parmi les hydrocarbures suivants : $C_{2}H_{2} ; C_{5}H_{12} ; C_{5}H_{8} ; C_{3}H_{6}$et $C_{9}H_{20}$
3.1.Ecrire les formules semi- développées des hydrocarbures dont les noms suivants :
a) $2,3-diméthylhexane$ ; b) $2, 2,4-triméthylpentane$ ; c)$3, 4,5-triméthyloctane $;
d) $6-éthyl-2- méthyl-4- propylnonane$ ; e)$1-chloro 2-méthylpropane$ ; f)$3-bromo 4-éthyloctane$
g)$4-éthyl 3-méthylheptane$ ; h)$2,3-diméthylpentane$
On procède à la microanalyse d’un corps $A$ qui est un produit de substitution monochloré d’un alcane. Les pourcentages en masse trouvés pour les éléments $C$ et $Cl$ présent dans $A$ sont : $%C=45 ,86% $;
$%Cl= 45,21%$
3.2-Déterminer la formule brute du corps $A$.
3.3-Quelle est la formule semi développée de $A$ sachant que sa molécule possède deux groupes méthyle ? Nommer-le.
Lire attentivement ce texte avant de répondre aux questions
L’électricité se transporte facilement et rapidement. Des lignes électriques livrent l’électricité depuis la centrale électrique jusqu’aux zones de consommation. Le transport de l’électricité à l’échelle nationale est principalement assuré en très haute tension à $400 000$ volts via des lignes aériennes dites d’interconnexion.
Des opposants se manifestent de plus en plus fréquemment pour demander leur disparition du champ visuel, ce qui est toujours coûteux et parfois techniquement presque impossible. A l’échelle régionale ou locale, le transport est assuré en haute tension ($225000$ et $63000$ volts essentiellement) via des lignes qui, elles, peuvent être enterrées.
L’utilisation de la très haute tension permet de limiter les pertes en ligne dues à l’effet Joule ou aux effets électromagnétiques (effets capacitifs entre la ligne et le sol). Les pertes énergétiques dans les lignes à haute tension sont proportionnelles aux distances parcourues par le courant électrique.
1.1. Donner un titre à cette
1.2. Donner le sigle (ou) abréviation des mots soulignés du texte. Préciser la valeur des tensions correspondantes
1.3. Sous quelle tension l’électricité livrée dans les habitations. Donner le sigle et la valeur de la tension
1.4. Expliquer pourquoi l’électricité est transportée sous haute tension
1.5. Qu’est-ce l’effet Joule ?
Les bobines du secteur primaire et secondaire d'un transformateur de laboratoire possèdent $N_{1}=500$ et $N_{2}=125$ spires. Les tensions efficaces mesurées sont $U_{1} =12.40V$ et $U_{2} =3.08V$
2.1. Calculer le rapport de transformation $m$ du transformateur.
2.2. Celui-ci est-il abaisseur et élévateur de tension ?
2.3. Que signifie les $4$ grandeurs de la relation ?
2.4. La bobine de $125$ spires est conservée au secondaire.
Calculer le nombre de spires de la bobine constituant la bobine du primaire pour obtenir un rapport de transformation de $2.0$
3.1. La tension de sortie de l'alternateur d'une centrale électrique est élevée au moyen d'un transformateur dont la plaque signalétique prote les indicateurs : $98 MVA /11.5 kV/136 kV/ 50Hz$
3.1.1. Que représente ces valeurs ?
$98 MVA$ : ....................................................................................................
$11.5 KV$ : ......................................................................................................
$136 kV$ : .......................................................................................................
$50 Hz$ : ........................................................................................................
3.1.2 Calculer le rapport de transformation m. Celui-ci est-il élévateur ou abaisseur de tension ? Quel est sa fonction ?
3.1.3. Calculer les intensités $I_{1}$ et $I_{2}$
3.2. Pour chaque situation, indiquer si le transformateur est élévateur ou abaisseur de tension et calculer son rapport de transformation.
3.2.1. Un poste de transformation électrique est passé de $20kV$ à $400 V$
3.2.2. Un poste de transformation électrique est passé de 230V à $23 kV$
AU TRAVAIL ET BONNE CHANCE

ou $Ag^{+}+Cl^{-}\longrightarrow AgCl$

ou $Ba^{2+}+SO_{4}^{2-}\longrightarrow BaSO_{4}$